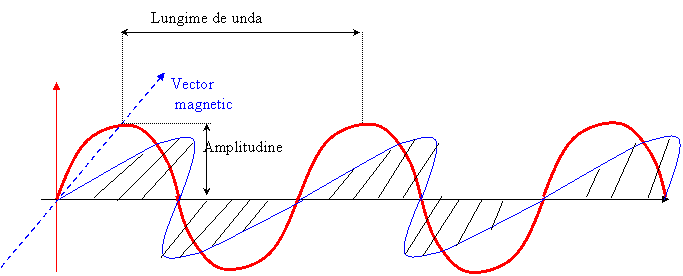
Fig.37. Reprezentare schematica a undei electromagnetice
l este distanta dintre doua puncte corespunzatoare 2p pe curba sinusoidala. Lungimea de unda se exprima ca orice lungime in submultiplii ai metrului, de obicei nm. Frecventa n reprezinta numarul de unitati de lungimi de unda care trec printr-un anumit punct, in unitate de timp. Frecventa se exprima in Hertzi (Hz), cicli pe secunda sau s-1.
Tabel.3 Domeniile spectrului in infrarosu

Intr-o molecula, pozitiile relative ale atomilor variaza in permanenta, existand un numar mare de moduri de vibratie si de rotatie, in jurul legaturilor din molecula. Pot exista foarte multe moduri de vibratie, chiar pentru molecule simple, dar ele pot fi reduse - prin insumare (sau diferenta) - la un numar mai mic si vor fi denumite moduri normale de vibratie ale anumitor atomi. Numarul de moduri normale de vibratie ale unei molecule depinde de numarul de atomi pe care-l contine si, deci, de gradele de libertate. in cazul unei molecule diatomice, sau triatomice simple, este relativ usor sa se defineasca natura vibratiilor si sa se faca legatura cu energiile de absorbtie. Acest tip de analiza este aproape imposibila, insa, pentru molecule ce contin un numar mare de atomi. Moleculele mari au un numar mare de centre de vibratie si, de asemenea, trebuie sa se tina cont de interactiunile dintre ele.[80,87]
Miscarea oricarui atom intr-o molecula va fi rezultatul vibratiei sau rotatiei si translatiei interne, care poate fi descompusa in componentele lor paralele eu axele x, y si z intr-un sistem de coordonate carteziene, in care un atom poate avea trei grade de libertate. Un sistem cu N nuclee (atomi) va avea, prin urmare, 3N grade de libertate. Pentru a defini miscarile posibile moleculare trebuie sa luam in considerare: 1. miscarea moleculei in spatiu (miscarea de translatie a centrului sau de greutate), 2. miscarea de rotatie a moleculei in jurul centrului de greutate, 3. miscarea fiecarui atom in raport fata de celalalt (vibratiile individuale). [80]
Totusi, pentru o molecula neliniara, sase din aceste grade de libertate corespund translatiei si rotatiei moleculei ca un intreg si, prin urmare, are frecventa de vibratie zero, astfel ca exista 3N-6 grade de libertate vibrationale sau moduri de vibratie normale, Pentru moleculele liniare, ca cea de dioxid de carbon, rotatia in jurul axei moleculare nu schimba pozitia atomilor si sunt necesare numai doua grade de libertate pentru a descrie orice rotatie. Prin urmare, moleculele liniare au 3N-5 vibratii normale sau moduri normale de vibratie. Teoretic, pentru un lant polimer infinit lung, exista numai trei translatii si o rotatie vor exista 3N-4 grade de libertate vibrationale. Fiecarui mod normal ii corespunde o curba de energie potentiala. Orice vibratie se poate considera o armonica; diferentele dinte nivelele de energie ale unui mod dat sunt egale, ceea ce inseamna ca nu apare decat o banda de absorbtie pentru un mod normal de vibratie, pentru care apare o modificare a momentului de dipol.[80,87]
Fiecare mod normal consta din vibratii, desi nu apar in mod necesar deplasari semnificative pentru toti atomii din sistem. La excitare, moleculele trec de la nivelul de baza (ν=0) la primul nivel de excitare (ν=1), in majoritatea cazurilor. Aceste tranzitii se definesc ca fiind vibratii fundamentale, proprii, respectiv normale. Ele au loc in domeniul 400 -1000 cm-1 (25-2,5 μm), cu energiile corespunzatoare 1-10 kcal/mol. Numarul vibratiilor fundamentale depinde, asa cum s-a mentionat, de numarul gradelor de libertate ale moleculei, egal eu 3N-6. De obicei, molecula poate absorbi radiatia IR daca tranzitiile spre nivele superioare au loc cu modificarea momentului de dipol (numai astfel de tranzitii fiind permise). Din aceasta cauza, gruparile foarte polare dintr-o molecula, cum este cazul C=O, -NO2, -SO2, etc., prezinta absorbtii foarte intense, in timp ce gruparile nepolare, de tipul olefinelor substituite R2C=CR2 sau azoderivatii R-N=N-R, sunt inactive in spectrometria IR. Tranzitiile interzise in IR se pot decela in spectrele Raman. In domeniul energetic mentionat, pe langa vibratiile fundamentale, au loc vibratii armonice superioare, ν = n ν1, cu n = 1,2,3,, datorita tranzitiilor pe nivelele superioare, si vibratii combinate ν = ν1+ ν2. Asa cum s-a amintit, intensitatea lor este relativ mica. Vibratiile fundamentale se impart in : Vibratii de valenta sau de alungire ( se modifica cu distanta interatomica in directia legaturii) si vibratii de deformare unghiulara ( la care se modifica unghiul de legatura). Exista patru astfel de vibratii: de forfecare, de rotatie, de balansare (oscilatie intercalata) si de torsiune. [80,87]
Fig.40 Moduri de vibratie moleculara pentru o molecula care contine mai mult de doi atomi. Semnul + indica o miscare a planului paginii catre cititor; semnul - indica alungirea. [80,87]
Fig.42. oscilatii angulare ale CO2
Dintre factorii ce influenteaza forma benzilor de absorbtie din spectrele IR face parte si scala de timp caracteristic masuratorilor. Spectrometria in infrarosu este caracterizata, in general, printr-o scala scurta de timp (aproximativ 10-13 s), comparativ cu cazul RMN, a carui scala de timp este de ordinul a 10 -8-10 -5s. Intr-un strat dublu fosfolipidic, se produc miscari rapide, cum ar fi izomerizarea gauche/trans (5-10'9s) sau trans/gauche (2,5-10 -8s) si difuzie rotationala (10-8- 10 -10 s). Este de asteptat ca pentru proteine aceasta miscare sa fie eu cateva ordine de marime mai inceata, din cauza masei lor moleculare mari si a restrictiei exercitate de stratul dublu fosfolipidic.
In ATR, forma benzilor de absorbtie depinde de o serie de parametri, precum: lungimea de unda a radiatiei incidente, indicii de refractie, eficienta contactului dintre proba si suprafata IRE. Alegerea neadecvata a unghiului de incidenta, a naturii elementului reflectant intern si a grosimii probei conduce la obtinerea de spectre puternic distorsionate. Nici una dintre variantele practicate pana in prezent nu poate fi catalogata, in sine, buna sau rea. In scopul definirii conditiilor experimentale potrivite, trebuie luate in considerare combinarea lor si natura probei.
In functie de dispozitivul experimental utilizat, modificarile ce apar in forma benzilor de absorbtie pot fi mai mari sau mai mici. Este posibil, deci, ca distorsiunile observate sa fie datorate efectelor optice simple. in acelasi timp, daca se lucreaza la unghiuri de incidenta mult diferite de unghiul critic, spectrele obtinute prin ATR sunt foarte asemanatoare celor obtinute prin transmisie.
Datele experimentale obtinute utilizand spectroscopia FTIR au fost obtinute atat pe membrane celulare (culturi celulare) cat si pe membrane artificiale (lipozomi). Urmarirea caracterului fluid membranar utilizand metoda FTIR se face analizand gradul de ordine/dezordine care exista la nivel membranar , urmarind modificarea picurilor de absorbtie pentru diferite tipuri de legaturi C-H, C=C, C=O, O=P=O, etc. [90, 91, 92] Aceste modificari de fluiditate membranara, traduse prin modificari ale picurilor de absorbtie sunt urmare a factorilor biofizici (temperatura, pH, cationi) sau biochimice ( concentratii colesterol, sfingolipide, acizi nesaturati, agenti externi). Ca si expresie a modificarii fluiditatii membranare se poate urmarii gradul de peroxidare lipidica membranara care este rezultat al cresterii radicalilor liberi cat si al modificarilor extracelulare si citosolice ale Ph-lui. Peroxidarea produce alterarea asimetriei lipidice, polaritatii lipidelor, suprafetei membranare, proteinelor membranare si enzimelor. Spectrometria FT-IR poate fi folosita pentru a determina modificarile structurale ale continutului eritrocitar (fosfolipide, proteine, lactat si glucoza) cat si pentru modificarile de la nivelul plasmei sanguine.[94,95]
Principalele domenii de absorbtie IR pot fi cu usurinta interpretate: Radicalii metil (CH3), metilen(CH2), metiliden(=CH) corespund fosfolipidelor; hemoglobina (C=O, N-H) reprezinta aproximativ 80%, iar spectrina aproximativ 10% din proteinele eritrocitare; resturile carbohidrate (C-O) reprezinta lactatul din interior (sau posibil glucoza, in cazul diabeticilor).[96,97]
Analiza presupune substragerea spectrului specific apei pe intervalul 3030-2800cm-1 (+corectia pentru Hc) si urmarirea spectrului de absorbtie in zona de intindere a frecventei de absorbtie pentru =C-H care este intre 3012 pana la 3030cm-1. si zona de intindere pentru C-H care este intre 2800- 3030cm-1. [95,96,97]
Pana acum, privind stresul oxidativ la nivelul membranei eritrocitare sau facut diferite studii privind stresul de efort [94-98] sau diferite patologii cum ar fi psoriazisul [99,100] diabetul si hipertensiunea [101,102] rezultatele punand in relatie modificari de ordin structural membranar (prin diferite metode spectroscopice FTIR, EPR sau NMR) cu statusul patologic sau fiziologic particular.
|