CLASA HALOGENURI
10.1 Clasificare
I. SĂRURI HALOIDE NORMALE ANHIDRE sI HIDRATATE
Tipul AX Grupa halitului Halit NaCl
Silvina KCl
Villaumit NaF
Kerargirit AgCl
Tipul AX2 Grupa fluorinei Fluorina CaF2
Grupa lawrencitului Bischofit MgCl2∙6H2O
II. SĂRURI HALOIDE COMPLEXE, ALUMINO-FLUORURI
Tipul AmBX3∙xH2O Carnalit KMgCl3∙6H2O
III. SĂRURI ALUMINO-FLUORURI
Tipul octaedric izolat Criolit Na3AlF6
10.2 Grupa halitului
Contine minerale izotipe cu grupul spatial Fm![]() m, dintre care cel mai comun este halitul, NaCl, cu Z=4.
m, dintre care cel mai comun este halitul, NaCl, cu Z=4.
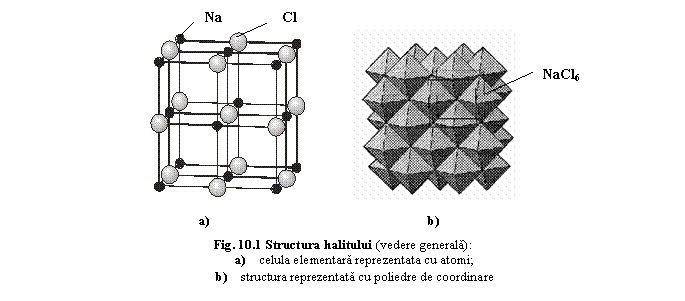
Structura reprezentata prin arhetipul structural "halit" (fig.10.1) (vezi si izotipism).
Ionii de Cl formeaza o retea cubica centrata pe fete (structura cubica compacta) în care Na ocupa toate cele patru pozitii interstitiale octaedrice ale împachetarii cubice compacte. Structura mai poate fi descrisa ca o intrepatrundere a doua retele cubice compacte de Na si Cl, cu o deplasare relativa egala cu ½ din diagonala cubului.
Coordinarea 6 (octaedrica)atât pentru Na cât si pentru Cl.
Celula elementara:a0=
 Legatura
Na-Cl: d(Na-Cl)=2,819 Å; legatura
aproape total ionica.
Legatura
Na-Cl: d(Na-Cl)=2,819 Å; legatura
aproape total ionica.
Proprietati fizice
Planele din structura halitului sunt plane de coeziune maxima. În acest plan situându-se legaturile Na-Cl (distanta Na-Cl în aceste plane este 2,819 Å). Aceasta explica trachtul si clivajul cubic perfect al halitului.
Sunt caracteristice tremiile, forme scheletice concave, constituite din suprapuneri rectangulare în descrestere progresiva, generate prin cresterea exagerata în directiile muchiilor, care apar la unele cristale de sare dezvoltate în conditii de suprasaturatie în lagunele zonelor tropicale. Aceste forme se dezvolta astfel deoarece colturile si muchiile cuburilor prezinta cel mai mare numar de valente libere.
Acest mineral este în general incolor, putând fi colorat allocromatic: coloratia cenusie se datoreaza particulelor de argila, coloratia galbena hidroxizilor de fier, culoarea rosie oxizilor de fier, iar coloratia bruna sau neagra substantelor organice. Un caz deosebit de interesant îl reprezinta culoarea albastra idiocromatica care se datoreaza transferului de electroni catre ionii de sodiu, transfer care conduce la aparitia de atomi neutri de sodiu care ies de sub influenta fortelor de legatura ale structurii si se plaseaza în diferite goluri ale structurii (defecte de retea). O astfel de coloratie idiocromatica se realizeaza în mod artificial când mineralul este supus actiunii fortelor radioactive (bombardament de radiatii γ).
10.3 Grupa fluorinei
Este reprezentata prin fluorina, CaF2
cu Z= , Fm![]() m
m
Structura (fig.10.2) poate fi descrisa ca o împachetare cubica compacta a ionilor de Ca în care toate cele opt pozitii interstitiale tetraedrice sunt ocupate de ioni de F. În celula elementara, ionii de Ca ocupa colturile si mijloacele fetelor, iar ionii de F ocupa centrele tuturor octantelor celulei.
Coordinare: Ca coordinat cubic de 8 F; F coordinat tetraedric de 4 Ca.
Legatura Ca-F: d(Ca-F)=2.362 Å; (rCa2++rF-=2,35 Å); potrivit criteriului electronegativitatii Pauling, 89% legatura ionica.
Celula elementara: a0

Proprietati fizice
Planele de coeziune maxima, cu distanta interatomica egala cu d(Ca-F) sunt planele , de aici clivajul octaedric perfect al fluorinei.
Trachtul este cubic, octaedric, rar dodecaedric romboidal. Prezinta macle de penetratie dupa axul 4, formate prin întrepatrunderea a doua cuburi.
Este incolora dar poate fi colorata allocromatic în galben, verde, violet, albastru, roz, rosu. Cristalele incolore pot deveni violete prin actiunea vaporilor de Ca metalic si a descarcarilor electrice, aceasta sugerând faptul ca, în unele cazuri, culoarea se datoreaza aparitiei în structura a atomilor de Ca sau F. Prin expunere la raze catodice se observa în general o fluorescenta violeta, cu o nuanta caracteristica albastra-verzuie. Fluorescenta se manifesta si la încalzire (termoluminiscenta).
|