Determinarea potentialului de coroziune
Se determina potentialele de coroziune pentru fier, aluminiu si zinc în medii corozive acide, neutre si bazice si supratensiunile corespunzatoare.
Coroziunea elecrochimica reprezinta procesul de distrugere al unui material metalic în contact cu un electrolit, prin reactii elctrochimice.
La interfata metal / electroli 727d321h t se desfasoara:
- procesul anodic de oxidare a metalului:
![]() (5.1)
(5.1)
- procesul catodic de reducere a unui depolarizant D din mediul coroziv:
![]() (5.2)
(5.2)
Depolarizantul este un acceptor de electroni din mediul coroziv ca de exemplu:
![]() ,
(în mediu acid, în absenta oxigenului) (5.3)
,
(în mediu acid, în absenta oxigenului) (5.3)
![]() ,
(în mediu neutru sau bazic,aerat) (5.4)
,
(în mediu neutru sau bazic,aerat) (5.4)
Reactia anodica si catodica se desfasoara simultan cu viteze egale la un potential numit potential de coroziune sau potential mixt.
Potentialul de coroziune se stabileste spontan la contactul metalului cu solutia de electrolit.
Valoarea
potentialului de coroziune este cuprinsa între valorile
potentialului reversibil de electrod al metalului ![]() si
depolarizantului
si
depolarizantului ![]()
![]() (5.5)
(5.5)
Marimile: ![]() (5.6)
(5.6)
![]() (5.7)
(5.7)
definesc polarizarea anodica ha si polarizarea catodica hc, care apare în momentul în care prin sistemul metal / mediu agresiv trece curentul de coroziune generat de procesul anodic si catod de coroziune.
Polarizarea sau supratensiunea reprezinta deplasarea celor doua potentiale de electrod reversibile, aproximate prin potentialul standard de electrod, fata de potentialul de coroziune. La polarizare anodica potentialul de electrod se deplaseaza spre valori mai electropozitive. La polarizare catodica potentialul de electrod al depolarizantului se deplaseaza spre valori mai electronegative.
Dupa cum rezulta din diagramele Evans, (figura 5.1) coroziunea poate fi sub control anodic (a), sub control catodic (b) si sub control mixt, controlat de reactia anodica si catodica (c). Diagramele Evans descriu variatia potentialului de electrod reversibil al metalului si depolarizantului în functie de densitatea de curent lgi.
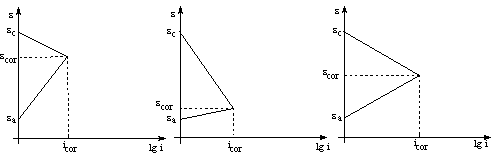
(a) (b) (c)
Fig. 5.1 Diagrama simplificata de coroziune, Evans.
a) control anodic, b) control catodic, c) control mixt.
Potentialul de coroziune si polarizarile corespunzatoare depind de natura si starea suprafetei metalului, de pH-ul mediului corespunzator si de temperatura.
Pentru masurarea potentialului de coroziune se alcatuieste o pila electrochimica prin asocierea metalului introdus în mediul coroziv cu un electrod de referinta si se masoara tensiunea electromotoare E a pilei.
E = e e eelectrod - ecor
referinta
Rezulta : ecor eelectrod - E (5.9)
referinta
Ca electrod de referinta se foloseste electrodul de calomel si în absenta acestuia electrodul de cupru.
Placute metalice de Fe, Zn si Al; electrod de referinta Cu / CuSO4 (1M), punte de sare, milivoltmetru electronic, pahar Berzelius.
Solutii apoase de HCl (pH < 6), NaCl (pH = 7) si de NaOH (pH > 8); hârtie abraziva, hârtie indicatoare de pH.
Se curata placutele metalice cu hârtie abraziva, se clatesc cu apa distilata.
Se face legatura între puntea de sare sau banda de hârtie de filtru umezita în solutia de CuSO4, cu un capat în solutia de CuSO4 si celalalt capat într-unul din mediile corozive, studiate, de exemplu în solutia acida.
Se introduce placuta metalica în mediul acid si electrodul constituit se conecteaza împreuna cu electrodul de referinta la bornele milivoltmetrului, astfel ca valoarea tensiunii electromotoare E sa fie pozitiva.
Se noteaza valoarea constanta a tensiunii electromotoare.
Se spala placuta metalica cu apa distilata, apoi se introduce pe rând în solutia neutra si în solutia bazica, repetând aceleasi operatii ca mai sus si notând de fiecare data tensiunea electromotoare indicata de acul voltmetrului.
Se procedeaza în acelasi mod si cu celelalte metale.
Observatii: - Dupa fiecare determinare placutele metalice se spala cu apa distilata.
- Dupa efectuarea tuturor masuratorilor metalul se scoate din solutiile corozive si se desfac legaturile de la milivoltmetrul electronic.
Datele experimentale si ulterior si cele
calculate se trec într-un ![]() tabel de forma:
tabel de forma:
|
Metal / mediu agresiv |
E, V |
ecor V |
ha V |
hc V |
Observatii |
Se scriu lanturile electrochimice ale elementelor galvanice alcatuite din electrodul metalic de lucru si electrodul de referinta, ca de ex:
(-) Fe / HCl (1 M) // CuSO4 (1M) / Cu (+)
Se calculeaza: potentialul de coroziune ecor pentru fiecare metal, în fiecare mediu coroziv cu relatia (5.9);
pentru electrodul de
referinta: ![]() sau
sau ![]() ).
).
Se calculeaza polarizarea anodica ha si polarizarea catodica hc cu relatiile (5.6) si (5.7).
Se folosesc urmatoarele valori ale potentialelor de electrod:
![]()
|