Introducere in studiul chimiei organice
Definitia chimiei organice
In 1809 J. Berzelius realizeaza un tratat de chimie in care clasifica substantele in : - substante organice ( provenite din mediul animal si vegetal )
substante anorganice ( provenite din mediul mineral )
Clasificarea nu are la baza un criteriu stiintific, ci se bazeaza pe observatii empi-rice. Introduce notiunea de forta vitala, forta inaccesibila omului, ce sta la baza formarii substantelor organice. Teoria vitala arata imposibilitatea crearii sub- stantelor organice de catre om si a dominat prima treime a secolului al XIX-lea.
In 1828 Wöhler realizeaza prima sinteza organica, printr-o simpla incalzire, transformand cianatul de amoniu (sare tipic anorganica) in uree diamida H2CO3- compus tipic organic).
![]()
![]() NH4NCO t0C H2N
NH4NCO t0C H2N
cianat de amoniu
![]()
H2N
uree
Reactia este o reactie de izomerizare, cei doi compusi fiind substante izomere, substante cu aceeasi formula moleculara, dar formule structurale diferite.
Experienta lui Wöhler arata ca obtinerea substantelor organice este accesibila omului, nefiind necesara pentru aceasta o forta de natura divina, ceea ce a deschis calea sintezelor organice.
In aceste conditii definitia pe care a dat-o Berzelius chimiei organice nu era corecta. Analiza substantelor organice arata prezenta cu preponderenta a atomului de carbon, atom pe care chimistii il pun la baza chimiei organice. Conform acestei teorii chimia organica este chimia carbonului. Aceasta definitie este partial corecta deoarece :
- exista multi compusi ai carbonului de natura anorganica ( H2CO3 si sarurile sale, CO2, CO ).
- exista multi compusi organici care in molecula lor nu prezinta atomi de carbon ( hidroxil amina H2N-OH, hidrazina H2N-NH2 ).
Analiza compusilor organici duce la concluzia prezentei alaturi de atomii de carbon al unui alt atom si anume atomul de hidrogen.
Compusii organici ai hidrogenului cu carbonul poarta denumirea de hidrocarburi. Analizele moderne arata ca teoretic si in mare parte practic, toti compusii organici pot fi sintetizati din hidrocarburi, acesti compusi denumindu-se derivati ai hidrocarburilor.
Derivatii hidrocarburilor: compusi organici rezultati prin inlocuirea unuia sau mai multor atomi de hidrogen cu atomi sau grupuri de atomi ai elementelor organogene organizati in functiuni.
Elemente organice : elemente care se gasesc in compusii organici, sunt nemetale C, H, O, N, S, P, X ( halogeni : F ,Cl, Br, I )
,,Organogene'' = dau nastere la compusi organici.
|
Functiunea |
Derivat | ||
|
X ( halogen ) |
R-X (derivat halogenat ) |
CH3-Cl (clorura de metil) |
|
|
OH (hidroxil) |
R-OH (alcool) R'-OH (enol) AR-OH (fenol) |
Derivat hidroxilic |
CH3-CH2-OH (alcool etilic) CH2=CH-OH (alcool alilic) C6H5- OH (fenol) |
|
NH2 (amina) |
R-NH2 (amina) |
CH3-NH2 (metil amina) |
|
Chimia organica - chimia hidrocarburilor si a derivatilor acestora.
Obiectul chimiei organice il constituie :
izolarea si purificarea substantelor organice.
stabilirea compozitiei si structurii lor.
cunoasterea proprietatilor lor si a posibilitatilor de transformare.
sinteza de laborator a compusilor organici ce prezinta importanta.
Ca urmare a nenumaratelor arderi, inclusiv respiratia animala, materia organica este degenerata oxidativ pana la dioxid de carbon si apa. Vegetatia retine dioxidul de carbon, il transforma in prezenta apei si a razelor luminoase in substante organice necesare plantei ( zaharide, proteine, grasimi ) cu eliminarea unei cantitati corespunzatoare de oxigen.
![]() nCO2 + nH2O lumina materie organica + nO2
nCO2 + nH2O lumina materie organica + nO2
![]()
![]() Acest
proces este catalizat de pigmentul verde al plantei ( clorofila ) si dirijat de
enzimele vegetale pe cai specifice. Substantele organice rezultate din
fotosinteza servesc la dezvoltarea plantei hrana pentru animale intretinerea si dezvoltarea
organism 252g66c ului animal. Unele substante sunt transformate in produsi necesari
celulei animale, altele sunt transformate furnizand energie organismului.
Acest
proces este catalizat de pigmentul verde al plantei ( clorofila ) si dirijat de
enzimele vegetale pe cai specifice. Substantele organice rezultate din
fotosinteza servesc la dezvoltarea plantei hrana pentru animale intretinerea si dezvoltarea
organism 252g66c ului animal. Unele substante sunt transformate in produsi necesari
celulei animale, altele sunt transformate furnizand energie organismului.
In sol exista pana la adancimi de cativa kilometri materiale organice sub forma de zacaminte, rezultatul transformarii chimice si biochimice anaerobe suferite de organismele vegetale si animale in epoci geologice departate.
Carbochimia ( chimizarea carbunilor ) a fost initiata in 1830 si petrochimia ( chimizarea petrolului )- aparuta un secol mai tarziu - constituie doua ramuri de baza a industriei organice de sinteza. Cantitati enorme de materie organica exista in apa marilor si oceanelor sub forma de organisme vegetale si animale de diferite genuri si grade de evolutie. Pe planeta noastra materia organica apare foarte raspandita :
In biosfera, plante superioare si majoritatea speciilor animale.
In hidrosfera, plante inferioare, animale, plancton.
In litosfera, zacaminte de petrol, carbune, gaze naturale.
![]()
![]()
![]()
![]() Plante O2
Plante O2
![]()
![]()
![]() carbune
carbune
![]()
![]() petrol
petrol
![]()
![]() H2O + CO2 animale
H2O + CO2 animale
![]()
Substante organice
2. Izolarea si purificarea substantelor organice
Caracterizarea unui compus organic incepe intotdeauna cu stabilirea compozitiei sale. Pentru aceasta, compusul organic este mai intai izolat din mediul din care a aparut ( mediul de reactie ), apoi purificat pentru indepartarea oricaror urme de substanta straina.
Izolarea si purificarea compusilor organici se poate face cu o gama foarte larga de metode fizice, fizico-chimice, biochimice, chimice. Exemplu : sublimarea, distilarea, cristalizarea, extractia.
Sublimarea : operatia de purificare bazata pe proprietatea unor substante solide de a sublima, de a trece prin incalzire direct in faza gazoasa, fara a se topi. Condensarea vaporilor rezultati conduce la o masa de cristale ( nu de lichid ) cu o puritate superioara probei initiale. Folosirea sublimarii este limitata numai la substantele care au proprietatea de a sublima.
Distilarea : metoda de izolare a compusului organic dintr-un amestec, de obicei lichid, alcatuit din mai multi compusi ( componenti ). Se bazeaza pe diferenta dintre punctele de fierbere ale componentelor din amestec. Se incalzeste amestecul intru-un vas de distilare, vaporii rezultati prin incalzirea amestecului la diferite temperaturi, sunt condensati si lichidele obtinute sunt culese separat.
Se poate participa in diferite variante de lucru in functie de valoarea diferentei punctelor de fierbere ale componentilor amestecului.
Distilarea fractionata simpla : pentru diferente mari ale punctelor de
fierbere ( 0 -
Distilare fractionata cu coloane de distilare : pentru diferente mici ale punctelor de fierbere ( 5 -100 C ).
Distilare fractionata la presiune scazuta, eventual cu coloana de distilare
( 1 - 5
Cristalizarea ( metoda de fractionare a componentelor unui amestec ) : se bazeaza pe diferenta de solubilitate a componentelor unui amestec intr-un dizolvant oarecare, la o temperatura apropiata de punctul sau de fierbere, se obtine o solutie saturata care prin racire conduce la o masa de cristale pure.
Extractia : aplicata atat lichidelor cat si solidelor, permite separarea unui component dintr-un amestec oarecare pe baza solubilitatii sale selective in anumiti solventi.
Rezultantul acestor operatii de purificare este urmarit prin intermediul unor marimi caracteristice compusilor organici numite caracteristici fizice (punctul de topire pentru substantele solide si indicele de refractie al lichidelor).
Cand dupa doua operatii de purificare, valoarea constantelor fizice nu se modifica, atunci substanta izolata este suficient de pura pentru a fi supusa investigatiilor analitice.
Activitate experimentala
Distilarea unui amestec de substante organice.
Se prepara in prealabil un amestec de acid acetic si tetraclorura de carbon in
proportie de 1:1. Fractionarea amestecului se poate realiza in doua moduri :
- in balonul Wurtz se introduce o cantitate de amestec egala cu ½ din capacitatea balonului si cateva bucati de portelan poros pentru omogenizarea fierberii. Se monteaza apoi termometrul, a carei scala sa fie astfel aleasa incat sa poata masura cel mai ridicat punct de fierbere al componentilor amestecului, avand grija ca bazinul cu mercur sa ajunga pana in dreptul tubului lateral al balonului de distilare. Se ataseaza apoi refrigerentul, se alimenteaza cu apa si la iesire se plaseaza vasul de culegere.
Se regleaza sursa de incalzire ( lampa cu
gaz sau sursa electrica ) astfel incat fierberea amestecului sa nu fie
violenta. Se noteaza temperaturile la care cei doi componenti vor distila si se
va masura cu un cilindru gradat cantitatea din fiecare component. Se stabileste
randamentul distilarii ( tetraclorura de carbon are punctual de fierbere
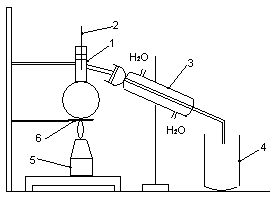 1 balon Wurtz
1 balon Wurtz
2 termometru
3 refrigerent racit cu apa
4 vas de culegere a distilari
5 lampa de incalzire
6 sita de azbest
Distilarea fractionata simpla folosita pentru prelucrarea unor cantitati mici de amestecuri ( 3 - 5 ml ).
Amestecul
supus distilarii este introdus intr-o eprubeta la care s-a atasat un manson de
cauciuc etans, un tub obisnuit de sticla cu rol de refrigerent, avand diametrul
interior mai mare cu 1-
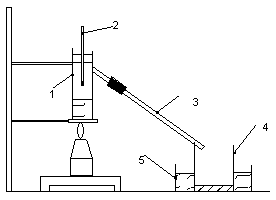
1 eprubeta cu tub lateral
2 termometru
3 refrigerent racit cu aer
4 vas de culegere
5 baie de racire a vasului de culegere
Purificarea acidului benzoic prin sublimare :
- Se introduc 100 ml apa si 2g acid benzoic impur intr-un vas Erlenmayer de circa 300ml capacitate.
- Se incalzeste amestecul pana la fierbere, cand se observa distilarea totala a acidului benzoic.
- Se filtreaza solutia fierbinte cat mai repede posibil.
- Filtrantul cules se imparte in doua parti egale : una va fi lasata sa se raceasca lent ( 10 - 15 min.), cealalta va fi racita rapid cu un jet de apa rece. In ambele se formeaza cristale de acid benzoic. In portiunea de solutie racita rapid se vor forma microcristale cu forma aciculara, iar in cealalta se vor forma cristale mari, bine determinate, vizibile cu ochiul liber.
Determinarea punctului de topire :
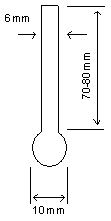
Intr-un tubusor capilar se introduce o cantitate mica de substanta solida uscata in prealabil si bine maruntita. Acesta se ataseaza de tija termometrului prin adeziune sau cu ajutorul unui inel de cauciuc. Eprubeta se scufunda intr-o baie de incalzire si se fixeaza cu o clema de stativ.
Se incalzeste si se urmareste atent cresterea temperaturii, notand valoarea la care faza solida din tubusorul capilar se topeste, devenind lichida.
1 eprubeta
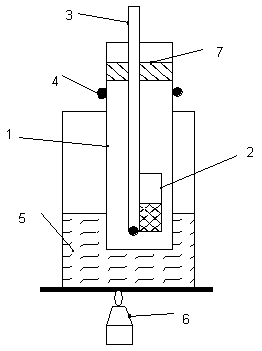 2 capilar inchis la un capat
2 capilar inchis la un capat
3 termometru
4 clema de fixare
5 baie de incalzire
6 lampa de incalzire
7 dop de pluta
Ca lichid de incalzire in baie se poate folosi :
- apa ( pentru
substantele cu punct de topire pana la 90-
- ulei de parafina sau glicerina ( pentru substante cu punct de fierbere pana
la 150-
- acid sulfuric ( pentru temperaturi mai mari ).
Experienta se poate realiza pentru diferite substante :
naftalina cu punct de
topire
a-naftilamina
cu punctul de topire
metadinitrobenzen cu
punct de topire
acid benzoic cu punct
de topire
uree cu punct de topire
acid salicilic cu
punct de topire
3. Compozitia substantelor organice
Desi compusii organici au un numar impresionant, ei sunt alcatuiti dintr-un numar relativ restrans de elemente chimice denumite elemente organogene
( C, H, O, N, S, halogeni ), nemetalele aflate in S.P. in coltul din dreapta.
Analiza elementala a substantelor organice
Prezenta in substantele organice a elementelor organogene se determina baza analizei chimice. Dupa purificare, substanta organica este supusa analizei elementale calitativa si cantitativa.
Analiza elementala calitativa urmareste identificarea speciilor de atomi care compun substanta organica cercetata. Substanta organica este supusa unor transformari chimice simple ai caror produsi finali sunt specifici si usor de identificat.
Exemplu : carbonul impreuna cu hidrogenul se identifica prin incalzire pana la descompunerea unei probe de substanta cu oxid de cupru ( CO ) cu formarea de CO2, a apei din carbonul si hidrogenul din substanta si oxigenul din agentul oxidant :
![]() Substanta ( C,H ) + CO CO2 + H2O + Cu
Substanta ( C,H ) + CO CO2 + H2O + Cu
Celelalte elemente organogene ( N,S, X ) sunt identificate dupa descompunerea termica a substantei in prezenta de sodiu cu formarea unor compusi anorganici usor de identificat prin reactii simple, specifice :
![]() Substanta ( C,H,N,S,X ) + Na NaCN + Na2S +NaX
Substanta ( C,H,N,S,X ) + Na NaCN + Na2S +NaX
in substantele organice, oxigenul nu se identifica ca element.
Analiza elementala cantitativa : dozeaza cu metode corespunzatoare elementele identificate anterior, cu exceptia oxigenului care se dozeaza ca diferenta.
Metodele folosite sunt arderile ( combustiile ) in care se formeaza
CO2 din carbon,
apa din hidrogen,
SO2 din sulf,
azot elementar din azot.
Rezultantul ei se exprima in procente si reprezinta formula procentuala a substantei.
Identificarea carbonului.
Se ia o
eprubeta uscata, prevazuta cu un dop prin care trece un tub de sticla indoit in
unghi drept, in care se amesteca 0,1 -
Se astupa eprubeta si se fixeaza pe un stativ in pozitie orizontala, capatul liber al tubului se introduce pana aproape de baza unei eprubete ce contine solutie diluata de hidroxid de calciu ( Ca(OH)2 ). Se incalzeste amestecul din ce in ce mai mult.
- La inceput se barboteaza aerul, apoi se dezvolta dioxidul de carbon :
![]() Substanta (C) + 2CuO CO2 + 2Cu
Substanta (C) + 2CuO CO2 + 2Cu
- Dioxidul de carbon se pune in evidenta prin formarea carbonatului de calciu, insolubil in apa.
![]()
![]() CO2 + Ca(OH)2 CaCO3 + H2O
CO2 + Ca(OH)2 CaCO3 + H2O
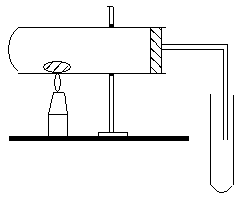
Identificarea hidrogenului.
Pe partile reci ale eprubetei se depun picaturi mici de apa, ce se formeaza prin oxidarea hidrogenului din substanta.
Ca(OH)2
![]() Substanta (H) + CO H2O + Cu
Substanta (H) + CO H2O + Cu
Mineralizarea substantei : intr-un tubusor de combustie se introduc substanta cu o bucatica de sodiu neoxidat si uscat pe hartie de in. Se prinde tubusorul intr-un cleste de lemn si se incalzeste treptat la flacara unui bec, mai intai in zona unde se afla bucatica de sodiu, iar dupa topirea ei si in zona substantei . Dupa ce substanta a ars, se incalzeste tubusorul pana la rosu si in aceasta stare se arunca intr-un pahar cu apa distilata. Se acopera cu o sticla de ceas. Se filtreaza solutia si se imparte filtrantul in trei parti egale, in vederea identificarii N, S si halogenilor.
 Identificarea azotului.
Identificarea azotului.
Intr-o eprubeta se introduc 3 - 4 ml din filtrantul de mai sus, 2 - 3 picaturi dintr-o solutie proaspata de sulfat de fier (II) 20% si 2 -3 picaturi solutie de clorura de fier (III). Se incalzeste pana la fierbere. Se aciduleaza cu 2 - 3 ml solutie de acid clorhidric :
- daca substanta contine azot putin se formeaza un precipitat verde albastrui.
- daca continutul in azot este mare se formeaza un precipitat albastru de hexacianoferat (III) sau albastru de Berlin Fe4[Fe(CN)6]3
Transformari chimice
- sodiul cu carbonul si azotul formeaza bromura de sodiu ( NaCN )
![]() Substanta
(C,N) + Na NaCN
Substanta
(C,N) + Na NaCN
- cianura de sodiu reactioneaza cu sulfatul de fier (II) si formeaza cianura de fier
![]() 2NaCN +FeSO4 Fe(CN)2 + Na2SO4
2NaCN +FeSO4 Fe(CN)2 + Na2SO4
- cianura de fier (II) cu exces de cianura de sodiu formeaza hexacianoferatul (II) de sodiu.
![]() Fe(CN)2 + 4NaCN Na4 [Fe(CN)6]
Fe(CN)2 + 4NaCN Na4 [Fe(CN)6]
- in prezenta ionilor de fier (III), hexacianoferatul (II) de sodiu formeaza albastru de Berlin sau hexacianoferatul (II) de fier (III)
![]() Na4 [Fe(CN)6] + 4FeCl3 Fe4[Fe(CN)6]3 + 12NaCl
Na4 [Fe(CN)6] + 4FeCl3 Fe4[Fe(CN)6]3 + 12NaCl
Identificarea sulfului :
Intr-o eprubeta se introduc 5 ml filtrat de la mineralizarea substantei sodiu si 1 ml de solutie apoasa de acetat de plumb. Daca substanta a avut sulf se formeaza un precipitat negru, sulfura de plumb. Substanta reactioneaza cu sodiu cu formarea sulfurii de sodiu.
![]() Substanta (S) + 2Na Na2S
Substanta (S) + 2Na Na2S
![]() Na2S +Pb(CH3COO)2 PbS + 2CH3COONa
Na2S +Pb(CH3COO)2 PbS + 2CH3COONa
Identificarea halogenilor :
- Intr-o eprubeta se introduc 5 ml filtrant de la mineralizarea substantei de sodiu. - Se aciduleaza cu acid azotic care nu contine halogeni.
- Se fierbe 1-2 min.
- Se raceste.
- Se adauga 1 ml solutie 5 % azotat de argint.
Daca substanta analizata contine halogeni se formeaza un precipitat de halogenura de argint :
![]() Substanta (X) + Na Na
Substanta (X) + Na Na
![]()
![]() Na + AgNO3 NaNO3 + AgX
Na + AgNO3 NaNO3 + AgX 

Formule procentuale, empirice, brute, moleculare
Rezultatul analizei elementelor cantitative se exprima sub forma de compozitie procentuala. Fie :
s cantitatea de substanta supusa combustiei
a cantitatea de CO2 ( dioxid de carbon ) rezultata in urma arderii, in conditiile in care tot carbonul a trecut in Dioxid de carbon
b cantitatea de apa rezultata
s a b
![]()
![]()
![]()
![]()
![]() Fp Fe Fb FM
Fp Fe Fb FM
Orice formula chimica ne ofera doua tipuri de informatii :
Calitative : ne arata speciile de atomi componente ale moleculei organice comune tuturor formulelor chimice.
Cantitative : informatii caracteristice fiecarui tip de formula chimica.
Formula procentuala Fp - aspectul
cantitativ ne arata cota de participare numerica a fiecarei specii de atomi la
formarea a
Determinarea C % : 1mol CO2 (44g).1 at g C (12g)
a g CO2.x g C
![]()
x = 12a / 44 => x = 3a/11
1g
substanta3a /
100g substanta C %
![]()
C% = 3a /11s * 100 C% = 300a / 11s
H % : 1mol H2O (18g).2 at g H (2g)
b g H2Oy g H
![]()
y = 2b / 18 => y = b/9 g H
s g
substantab /
100g substanta H %
![]()
H% = 100b / 9s
In mod analog se determina continutul procentual al tuturor celorlalte elemente organice, cu exceptia oxigenului care se determina prin diferenta :
O % = 100 - ( C% + H% + .. )
![]()
Rezultatul se scrie sub forma Fp : C :
H :
![]()
O :
Determinarea formulei empirice ( Fe ), aspectul cantitativ ne arata raportul masic in care se gasesc speciile de atomi componente ale moleculelor organice. Formula se determina prin impartirea procentelor de la formula procentuala la masele atomilor respectivi ( AC=12, AH=1, AO=16, AS=32, AF=18 ). Se obtin indicii formulei empirice.
Determinarea formulei brute (Fb) aspectul cantitativ ne arata raportul numeric (atomic) in care se gasesc speciile atomice componente ale moleculei organice. Pentru aceasta se impart indicii formulei empirice la cea mai mica valoare a lor, rezultatul il reprezinta indicii formulei brute.
Determinarea formulei moleculare (FM) aspectul cantitativ il reprezinta numarul real din fiecare specie de atomi componente ale compusului organic. Formula moleculara este un multiplu al formulei brute, factorul de multiplicare fiind n.
M
![]() n
=
n
=
suma maselor atomice ale elementelor componente tinand cont de indicii Fb
Gazele rezultate in urma combinatei sunt trecute prin vase spalatoare care au rolul de a retine selectiv si cantitativ componentele.
H2O este retinuta de vasul spalator cu:
acid sulfuric(H2SO4) concentrat: retinerea este fizica, avand loc diluarea solutiei, aplicatia se bazeaza pe proprietatile higroscopice ale acidului sulfuric.
Clorura de calciu(CaCl2) anhidra: retinerea este chimica cu formarea clorurii de calciu hexahidratate(CaCl2*6H2O)
CO2 este retinut de vasul spalator cu :
Lapte de var ( solutie de Ca(OH)2, retinerea este chimica si se formeaza precipitatul de carbonat de calciu ( CaCO3 )
![]()
![]() CO2 + Ca(OH)2 CaCO3 + H2O
CO2 + Ca(OH)2 CaCO3 + H2O
Solutie de potasa caustica (KOH), retinerea este chimica
![]() 2KOH + CO2 K2CO3 + H2O
2KOH + CO2 K2CO3 + H2O
Excesul de oxigen rezultat in urma combustiei este retinut de vasul spalator cu pirogalol ( 1,2,3 - trihidroxi benzen ), retinerea este chimica si se bazeaza pe sensibilitatea pirogalolului fata de oxigen.
In toate cazurile cresterea masei vasului spalator se datoreaza componentelor din gazele de combustie, datorata retinerii.
Nu orice insiruire de simboluri chimice si indici reprezinta o formula a unei substante organice. Pentru verificarea valabilitatii unei formule moleculare se folosesc doua principii :
Principiul paritatii : Pentru o substanta reala suma tuturor covalentelor elementelor componente tinand cont de indicii formulei moleculare trebuie sa fie un numar par.
Principiul nesaturarii echivalente : nesaturarea echivalenta este o masura a gradului de nesaturare a unei substante. Poate fi folosit pentru determinarea validitatii unei formule moleculare.
Pentru o substanta de formal:
CaHbOcNdXe,
indicele de nesaturare se calculeaza :
(2a+2) - (b - d +e)
![]() N.E.=
N.E.=
2
Pentru o substanta reala indicele de nesaturare trebuie sa fie intreg, pozitiv, inclusiv zero.
Observatie - in exprimarea valorii indicelui de nesaturare echivalenta nu intra substantele divalente.
4. Structura compusilor organici
Modul de organizare al atomilor elementelor componente in ansamblul moleculei poarta denumirea de structura a moleculei. Pentru a cunoaste structura unui compus organic este necesara cunoasterea naturii atomilor elementelor componente, natura legaturilor ce se realizeaza intre atomi, geometria atomilor si a legaturilor .
Intre atomii elementelor organice se stabilesc legaturi covalente ( atomii elementelor organice sunt atomi de nemetale). Alaturi de legaturile covalente intalnim legaturi covalent - coordinative ( in special in cazul compusilor de tip amoniu ) si chiar, dar mai rar, legaturi ionice. Nu se intalnesc legaturi metalice.
a.) Legatura covalenta in compusii organici
La formarea legaturilor covalente participa atomi atat in stare fundamentala ( H, X, N, S ) cat si in stare hibridizata ( C, N, O ). Legatura covalenta este legatura ce se realizeaza prin punerea in comun a cate unui electron de catre fiecare atom de nemetal participant la formarea legaturii.
Atomul realizeaza un numar de legaturi covalent egal cu numarul orbitalilor mo- noelectronici neparticipanti la formarea legaturi.
In cazul in care atomul considerat se afla in stare hibridizata, legatura se formeaza astfel :
- prin intermediul orbitalilor hibrizi se formeaza numai legaturi covalente σ ( nu- marul legaturilor σ = numarul orbitalilor hibrizi monoelectronici)
- prin intermediul orbitalilor p puri ( nehibridizati ) se formeaza legaturi covalente π ( numarul legaturilor covalente π = numarul orbitalilor π puri monoelectronici )
Daca atomul se afla in stare fundamentala, el realizeaza prin intermediul orbitalilor monoelectronici numai legaturi sigma.
In compusii organici exista legaturi :
- simple ( o legatura covalenta simpla )
- multiple - dubla ( o legatura sigma si o legatura π )
- tripla ( o legatura sigma si doua legaturi π )
b.) Atomul de carbon in compusii organici
Multitudinea compusilor organici se explica si prin faptul ca atomul de carbon participa la formarea de legaturi in stare hibridizata, este singurul care are puterea de incatenare ( proprietatea atomului unui element de a forma lanturi de atomi de carbon ).
Aceasta proprietate se explica prin faptul ca atomul de carbon isi are stratul de valenta foarte aproape de nucleu, unde are patru electroni, pe care ii distribuie astfel incat in nici una din starile de hibridizare nu prezinta un orbital complet ocupat. Aceasta asigura stabilitate maxima atomului de carbon hibridizat si simetrie maxima.
C(z=6) : 1s22s22p2
![]() E
E
![]()
![]()
![]()
|
|
|
|
|
|
||||||||||||||||
|
p |
|
|
|
|
p pur |
p pur | ||||||||||||||
|
C |
sp3 |
|
|
| ||||||||||||||||
|
C |
sp2 |
|
| |||||||||||||||||
|
|
C |
sp |
s
St. fundamentala
Diagrama energetica arata ca odata cu ridicarea cotei de participare energetica a orbitalilor s la formarea orbitalilor hibrizi energia orbitalilor hibrizi scade.
Tipul hibridizarii Cota de participare a Variatia energiei
a orbitalilor s orbitalilor hibrizi
![]()
Csp3 25%
Csp2 33,3% scadere
Csp 50%
Variatia energiei orbitalilor hibrizi : Csp3 > Csp2 > Csp
O legatura, sigma sau pi , formata de fapt din doi electroni, se reprezinta conventional printr-o liniuta ( - ).
O legatura dubla se reprezinta ( = ) iar o legatura tripla ( ≡ ).
Csp3 - simetrie tetragonala.
![]() Prezinta 4 orbitali hibrizi monoelectronici 4 legaturi covalente sigma
Prezinta 4 orbitali hibrizi monoelectronici 4 legaturi covalente sigma
![]() 4 legaturi simple.
4 legaturi simple.
![]() .
.
. C . (Csp3) - C - (Csp3 ce realizeaza 4 legaturi simple )
![]() .
.
![]() H H
H H
![]()
![]()
![]()
![]()
![]()
![]()
![]() H C H H C H CH4
H C H H C H CH4
H H
In toti compusii organici atomul de carbon este tetravalent , indiferent de natura hibridizarii.
![]()
![]() H H
H H
![]()
![]()
![]()
![]()
![]() H C C H C2H6 CH3 - CH3
H C C H C2H6 CH3 - CH3
H H
C sp2 simetrie trigonala
![]() Prezinta - 3 orbitali hibrizi monoelectronici 3 legaturi simple : 1 leg. dubla
Prezinta - 3 orbitali hibrizi monoelectronici 3 legaturi simple : 1 leg. dubla
2 leg. simple
![]() 1 orbital p pur 1 legatura π
1 orbital p pur 1 legatura π
![]() .
.
![]() C : C
═ ( atomul de Csp2 ce realizeaza 2 legaturi
simple si o
C : C
═ ( atomul de Csp2 ce realizeaza 2 legaturi
simple si o
. legatura dubla )
![]()
![]() H H
H H
![]()
![]() H2C
= CH2 ( etena ) C = C
H2C
= CH2 ( etena ) C = C
H H
![]() Prezinta 2
orbitali hibrizi monoelectronici ---> 2 legaturi sigma
Prezinta 2
orbitali hibrizi monoelectronici ---> 2 legaturi sigma
2 orbitali p puri ---> 2 legaturi pi
Realizeaza: a) - 1 legatura simpla
1 legatura tripla
b) - 2 legaturi duble
.
.C . , - C ≡ ( Csp a realizat o legatura tripla si o legatura simpla )
.
C2H2 HC ≡ CH ; H - C ≡ C - H
: C : , = C = ( Csp2 a realizat 2 legaturi duble )
CH2 = C = CH2
Atomul de carbon prezinta covalenta 4, atomul de hidrogen covalenta 1, atomul de oxigen covalenta 2, atomul de azot covalenta 3, atomul de halogen covalenta 1.
Atomul de azot
in compusii organici participa la formarea legaturilor covalente atat in stare
fundamentala, cat si in stare hibridizata, caz in care prezinta valoarea
N (Z=7): 1s22s22p3
![]() E
E
![]()
![]()
![]()
|
|
|
| ||||||||||||||||||
|
p |
|
|
||||||||||||||||||
|
|
p pur | |||||||||||||||||||
|
|
|
|
|
p pur | ||||||||||||||||
|
sp3 |
|
|
| |||||||||||||||||
|
sp2 |
|
| ||||||||||||||||||
|
|
sp |
s
Nsp3 reprezinta 3 orbitali hibrizi monoelectronici , 3 legaturi covalente simple.
..
. N . Nsp3 - simetrie de piramida turtita
.
![]() H
H
![]() CH3 - NH2 , H3C
- N
CH3 - NH2 , H3C
- N
H
Daca atomul de azot foloseste dubletul electroni neparticipant ca donator intr-o legatura covalenta coordinativa se modifica simetria in simetria tetragonala.
Nsp2 prezinta - 2 electroni sigma = > 2 legaturi sigma - 1 legatura dubla
1 legatura simpla
1 electron pi = > 1 legatura pi
![]() .. electroni dintr- un orbital hibrid
complet ocupat cu electroni
.. electroni dintr- un orbital hibrid
complet ocupat cu electroni
- N : ( dublet electronic neparticipant )
..
-N =
( N sp2 ce si-a realizat legaturile )
![]() Hibridizarea
Hibridizarea
|
|
|
|
| ||||||||||||||
|
p |
|
|
|
|
p pur | ||||||||||||
|
sp3 |
|
|
|
|
|||||||||||||
|
sp2 | |||||||||||||||||
|
| |||||||||||||||||
O (Z=8): 1s22s2 2p6
Atomul de oxigen prezinta, in stare
fundamentala, un numar de 6 electroni distribuiti: 2 in 2s si 4 in 2p.
In aceasta stare prezinta 2 orbitali semiocupati, deci valoarea
In stare hibridizata sp3,
prezinta 4 orbitale hibride, 2 complet ocupate cu electroni si 2 semiocupate - valoarea
Atomul de oxigen sp2 prezinta 3 orbitale hibride ( 3 complet ocupate, 1 semiocupat ) si un orbital p pur semiocupat. Prin intermediul orbitalului hibrid semiocupat se realizeaza o legatura covalenta σ, iar prin intermediul orbitalului p pur semiocupat, o legatura covalenta π. Atomul de oxigen sp2 realizeaza o legatura dubla (o legatura σ si o legatura π); el prezinta o simetrie trigonala.
Atomul de oxigen nu realizeaza hibridizare sp.
Concluzii
Atomii elementelor organogene, fiind atomi de nemetal, vor fi legati intre ei numai prin legaturi covalente.
In compusii organici atomii elementelor organice prezinta urmatoarele valori ale covalentei : C-4, H-1, N-3, S-2, P-3, X-1. Realizarea legaturilor simple si multiple implica urmatoarele valori ale covalentii maxime :
a) legatura simpla - toti atomii elementelor organice, indiferent de valoarea maxima a covalentei.
b)
Legatura dubla: atomii
elementelor organice care au valoarea
c)
Legatura simpla:
atomii elementelor organice care au valoarea
Toate covalentele atomilor componenti ai unei molecule organice satisfacute numai prin legatura covalenta. Aparitia legaturii covalente coordinativa se datoreaza folosirii de un atom a dubletelor electronice neparticipante ca donor intr-o legatura covalent-coordinativa. Aparitia structurii organice are la baza tocmai faptul ca atomii elementelor organice se unesc prin legaturi covalente.
Legatura covalenta prezinta o serie de caracteristici ce explica structura organica:
Este dirijata in spatiu pe directii bine determinate care se conserva in timpul existentei moleculei in care apare.
Fac intre ele unghiurile ale caror valori sunt constante pentru o substanta chimica data.
Atomii legati prin legaturi covalente sunt situati la distante definite si caracteristice.
Numai atomii legati cu legaturi covalente alcatuiesc molecule, compusii ionici nu sunt formati din molecule.
Un prim factor determinant al existentei structurii chimice organice il reprezinta existenta legaturii covalente, cu caracteristicile ei.
Un alt factor important care explica multitudinea de compusi organici este proprietatea pe care o are atomul de carbon de a forma lanturi in care exista zeci si chiar sute de mii de atomi de carbon. Aceasta proprietate, la acest nivel, o are doar atomul de carbon si poara denumirea de catene de atomi de carbon.
Intr-o catena, un atom de carbon realizeaza un anumit numar de legaturi cu alti atomi de carbon respectand tetravalenta atomului de carbon.
Tinand cont de numarul legaturi pe care un atom de carbon le poate realiza intr-o catena cu alti atomi de carbon, atomul de carbon poate fi:
nular :atomul de carbon ce nu realizeaza nici o legatura cu un alt atom de carbon
H
![]()
![]()
![]() H C H (CH4)
; CH3-O-CH3
H C H (CH4)
; CH3-O-CH3
![]()
H
secundar: realizeaza 2 legaturi cu alti atomi de carbon:
![]()
H3C-CH2-CH3
![]()
![]()
CH2=CH2
tertiar: realizeaza 3 legaturi cu alti atomi de carbon:
![]()
![]()
![]()
H3C - CH - CH3
CH3 H2C = CH - CH3
![]()
![]()
HC ≡ CH
cuaternar: realizeaza 4 legaturi cu alti atomi de carbon:
![]() CH3
CH3
![]()
![]()
CH3 - C - CH3 H2C = C = CH2
![]()
CH2
![]()
![]()
![]() H3C
H3C
![]() H3C
H3C
Pe langa proprietatea de a fi primar, secundar, o alta caracteristica a acestora cauza fundamentala e existentei compusilor organici, este proprietatea de incatenare.
Numai atomul de carbon prezinta aceasta proprietate in catena putand exista zeci, sute pana la sute de mii de atomi de carbon legati intre ei.
Tinand cont de natura hibridizarii, atomilor de carbon ce intra in componenta unei catene, aceasta poate fi:
saturata :contine numai atomi de carbon saturati, atomi de carbon hibridizati sp3
nesaturata : contine pe langa atomi de carbon sp3 si atomi de carbon nesaturati, C sp2 si sp, intre care se realizeaza legaturi multiple
Tinand cont de modul de dispunere a atomilor de carbon in ansamblul unei catene aceasta poate fi:
liniara:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() C
- C - C - C - C - C - C -
C
- C - C - C - C - C - C -
O astfel de catena daca este saturata contine numai atomi de carbon primar si secundar.
ramificata:
![]()
![]()
![]() C
C
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() C
- C - C - C - C - C - C -
C
- C - C - C - C - C - C -
![]()
![]()
![]() C C
C C
![]()
![]()
O structura saturata ciclica contine toate tipurile de atomi de carbon.
![]()
![]()
![]()
![]()
![]()
![]() C
C
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() C C C C
C C C C
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() C C C C
C C C C
![]()
![]()
![]()
![]()
C
![]()
![]()
Catenele ciclice saturate contin toate tipurile de atomi de carbon mixte
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() C
- C - C - C - C - C - C -
C
- C - C - C - C - C - C -
![]()
![]()
![]()
![]()
![]() C
C
Structura chimica organica este aspectul cel mai important al unei molecule deoarece ne arata modul de aranjare al atomilor in ansamblul spatial al moleculei si interactiunile reciproce dintre atomi.
Catene de atomi de carbon → aciclice → liniare - saturate
![]() - nesaturate
- nesaturate
→ ramificate - saturate
- nesaturate
ciclice → simple - saturate
- nesaturate
→ cu catena laterala - saturate
- nesaturate
Structura chimica organica explica proprietatile fizico - chimice ale acestora. Cunoasterea structurii permite identificarea substantei. Formula moleculara ( ea singura ) ofera foarte putine informatii structurale, la formula moleculara data pot exista o multitudine de compusi chimici. Fenomenul poarta numele de izomerie.
Izomeria este fenomenul prin care unei formule moleculare i se atribuie doua sau mai multe substante diferite.
FM C2H6O (2 izomeri ) → CH3 -O - CH3 ( dimetileter )
→ CH3 - CH2 - OH ( alcool etilic )
FM C3H6O are 9 izomeri
Determinarea structurii unui compus organic implica mai multe etape facandu - se pas cu pas, folosindu - se metode :
fizice
chimice ( analiza functionala si elementara )
fizico - chimice ( spectro - fotometrie in UV, RMN, RMQ )
Rezultatele analizei functionale sunt concretizate in formule structurale. Formulele structurale sunt reprezentari grafice ce scot in evidenta particularitatile structurale ale moleculelor respective.
- formule plane, obisnuite, nu redau imaginea spatiala a moleculelor, dar sunt
folosite datorita comoditatii.
- formule de proiectie sunt rezultatul proiectiei imaginilor spatiale ale moleculelor in planul hartiei. Redau imaginea spatiala ( schema moleculara )
H H
![]()
![]()
H - C - C - H
![]()
![]()
H H
- formule de configuratie redau dispozitia spatiala a substituentilor legati direct la atomul de carbon. Se foloseste un cod al liniilor pentru reprezentare.
i ) linie punctata pentru legaturi ce se afla in spatele foii de hartie
ii) linie continua pentru legaturi ce se afla in planul foii de hartie
iii) linie pana pentru legaturi ce se afla in fata planului foii de hartie, spre observator ( partea ingrosata spre observator )
![]()
![]() H H
H H
C ▬ H
![]()
![]()
![]() C ▬ H
C ▬ H
H H
- formule de conformatie indica aranjamentul geometric rezultat in urma rotirii atomilor de hidrogen in jurul axei de simetrie a atomilor de carbon.
![]()
![]() H H
H H
 C
C
![]()
H
H
![]()
![]()
![]() C
C
H H
- modele structurale reprezentari reale ale unor molecule organice confectionate din diferite materiale care incearca sa reprezinte particularitatile structurale ale compusilor
|