SPECTROMETRIE DE MASA
Spectrometria de masa permite masurarea maselor moleculare relative a unor compusi unitari, respectiv evidentierea anumitor specii atomice si grupari functionale existente in compusul analizat.
3.1. PRINCIPIUL DE BAZA
In spectrometrul de masa moleculele organice neutre sunt transformate in ioni, radicali si molecule neutre simple; ionii generati prin fragmentare sunt ulterior deviati in campuri magnetice si/sau electrice. Devierea ionilor este dependenta de masa si sarcina acestora (in cazul substantelor organice sarcina este de obicei 1). Cel mai simplu exemplu de spectrometru este cel cu impact electronic in care moleculele aflate in stare de vapori in vid inaintat sunt bombardate cu un fascicul electronic de inalta energie. In urma acestui proces rezulta ioni pozitivi de energie mare (ionul molecular sau ion parinte), care se poate fragmenta mai departe in ioni mai mici (fragmente ionice). Pierderea unui electron de catre molecula conduce la un radical cationic, denumit ion molecular:
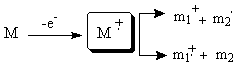
Ionul molecular ![]() se descompune de obicei intr-o pereche de fragmente: - un radical (m2 ) si un ion (m1+) sau
se descompune de obicei intr-o pereche de fragmente: - un radical (m2 ) si un ion (m1+) sau
- o molecula mica (m2) si un radical cationic (m1+
Ionii moleculari si fragmentele ionice sunt accelerati in camp electric si apoi separati prin deviere intr-un camp magnetic variabil in functie de masa si sarcina lor si genereaza un curent ionic proportional cu abundentele relative ale ionilor. Spectrul de masa este o reprezentare a abundentei ionilor in functie de valoarea raportului m/z (masa / sarcina). Majoritatea ionilor produsi au sarcina egala cu unitatea (z=1). In cazul acestora, cu cat masa este mai mica cu atat ionul este mai usor deviat in camp magnetic. Particulele neutre produse prin fragmentare, (molecule neincarcate electric, sau radicali), nu pot fi detectate direct in spectrometrul de masa.
In concluzie, un spectrometru de masa este un instrument care masoara masa unei molecule dupa ce aceasta a fost transformata in ioni. Pentru a nu se face confuzii reamintim ca nu se masoara direct masa moleculei ci mai exact raportul masa/ sarcina pentru un ion. In cazul in care sarcina este egala cu unu (z=1) acest raport corespunde cu masa moleculare (ionului) dar exista si cazuri in care z≠1.
Reamintim faptul ca deoarece moleculele sunt foarte mici nu se justifica masurarea masei in kilograme sau grame de aceea s-a ales ca unitate de masura Dalton-ul (unde 1 Da=1/2 din masa unui singur atom al izotopului 12C, prin conventie s-a atribuit pentru izotopul 12C masa de 12.000000 unitati de masa).
3.2. NOI TEHNICI UTILIZATE IN SPECTROMETRIA DE MASA.
Ionizarea cu electroni accelerati la un potential 70 eV, valoare aleasa deoarece asigura ionizarea oricarei molecule este un proces dur ce poate duce la o fragmentare intensa care lasa foarte putin sau deloc ion molecular. Deoarece este foarte important sa cunoastem masa moleculara a substantei investigate s-au dezvoltat tehnici de ionizare de energie joasa bazate pe ionizarea chimica (CI) si ionizarea de desorbtie.
Ionizarea chimica (CI) presupune formarea ionilor printr-un proces delicat de transfer de proton. Moleculele sunt expuse la un exces de gaz ionizat (de ex. metanul in forma protonata CH5+) cand are loc transferul protonului de la gazul reactant la o molecula cu formarea ionului pozitiv [M+H]+.
In conditii de CI se pot produce si ioni negativi prin transferul unui proton de la molecula analizata la un gaz reactant (sau ioni) cu formarea unui ion incarcat negativ [M-H]-. Prin coliziunea ionului negativ [M-H] - cu un fascicul de electroni de energie joasa, se formeaza un ion M- foarte intens.
Ionizarea de desorbtie este un proces prin care o molecula este evaporata de pe o suprafata si ionizata. Ionizarea se poate face printr-un proces de impact ce implica bombardarea probei cu atomi de viteza mare, ioni, fragmente de fisiune sau fotoni cu energie mare. In urma impactului proba acumuleaza energie, direct sau prin intermediul unei matrice, si conduce, pe ambele cai, la transformarea moleculei in ioni in faza gazoasa.
Cele mai importante metode de ionizarea de desorbtie sunt:
Cu ajutorul acestor tehnici domeniul de aplicabilitate al spectrometriei de masa a fost extins la: identificarea structurii acizilor nucleici, proteinelor oligozaharidelor, investigarea poluantilor de mediu, determinarea varstei si originii mostrelor in geochimie si arheologie, identificarea calitativa si cantitativa a unor compusi din amestecuri organice complexe.
3.3. DESCRIEREA APARATURII EXPERIMENTALE
Aparatura in spectrometria de masa este foarte variata, fiind functie de tehnica folosita in obtinerea, separarea, detectia si inregistrarea ionilor.
Schema de baza a unui spectrometru cu bombardament de electroni este prezentata in Schema 3.1.
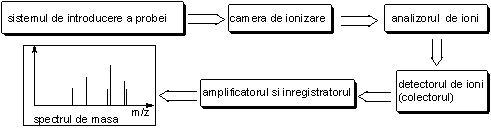
Schema 3.1
Principalele componente ale unui spectrometru de masa sunt:
1. Sistemul de introducere a probei:
Introducerea probei in camera de ionizare se poate realiza direct in cazul substantelor putin volatile sau instabile termic, respectiv indirect, pentru substante stabile termic, care la presiune moderata si temperaturi de aproximativ 300°C, se afla sub forma de vapori.
In cazul sistemelor cu introducere directa a probei cantitatea de substanta necesara inregistrarii spectrului de masa este foarte mica, de ordinul microgramelor (cca. 20 μg), in timp ce pentru sistemele cu introducere indirecta a probei sunt necesare cantitati mai mari de substanta 1-2mg. Sistemele cu introducere directa a probei se preteaza numai pentru inregistrari calitative deoarece metoda prezinta cateva dezavantaje:
- camera de ionizare trebuie curatata periodic;
- evaporarea neuniforma a probei genereaza schimbari ale raportului intensitatii diferitelor picuri de fragmentare.
2. Camera de ionizare
In camera de ionzare vaporii substantei analizate sunt bombardati cu un fascicul electronic produs de un filament din tungsten si accelerat sub o diferenta de potential de ≈ 75 eV. In aparatele clasice, unde ionii parcurg o distanta relativ mare pana la detector, se lucreaza la o presiune de ≈10-6 mmHg, deoarece in aceste conditii liberul parcurs mediu intre doua ciocniri ale particulelor aflate in stare gazoasa este de ≈ 1m. Astfel se exclude practic ciocnirea ionilor care ar duce la transfer de atomi sau grupari, complicand interpretarea spectrelor. In aparatele cu analizor cuadrupolar (vezi mai jos) presiunea poate fi mult mai ridicata, deoarece parcursul ionilor este scurt. In urma impactului rezulta ioni pozitivi, radicali si fragmente ionice. De asemenea in timpul impactului electronic este posibila si formarea de ioni negativi, dar eficienta acestor procese este mult mai mica fata de producerea de ioni pozitivi. Detectarea ionilor negativi se poate realiza prin inversarea polarizarii analizorului.
Un alt proces ce conduce la formarea de ioni este ionizarea chimica. Aceasta are loc la presiuni mai mari ale gazului molecular, cand o parte dintre ionii produsi reactioneaza chimic cu moleculele neutre.
3. Analizorul de ioni
In aceasta zona are loc analiza ionilor in functie de masa acestora. Analiza se poate realiza cu ajutorul unui camp magnetic, care diferentiaza ionii in functie de raportul m/z. Modificarea traiectoriei ionilor, astfel incat acestia sa focalizeze in colector si sa fie inregistrati, se poate realiza prin modificarea potentialului electric de accelerare a ionilor, sau a campului magnetic.
Inainte de analiza fascicolului de ioni in camp magnetic este necesara focalizarea fascicolului, realizata de un analizor electrostatic. Analizorul electrostatic focalizeaza ioni de aceeasi energie cinetica, oricare ar fi valoarea m/z, dupa care un analizor magnetic separa ionii cu valori m/z diferite. Un astfel de spectrometru se numeste cu dubla focalizare si poate atinge rezolutii de pana la 1:60.000 de unitati de masa.
Un alt tip de analizor este cel cuadrupolar, constituit din patru bare metalice paralele pe care este aplicat un potential oscilant +U+Vcosωt. Traiectoria ionilor sub actiunea acestui potential este sinusoidala, dependenta de potentialul aplicat. Pentru valori date ale lui U si V, numai ionii cu o valoare bine determinata m/z vor traversa intreaga lungime a filtrului. Toti ceilalti ioni vor avea oscilatii instabile, vor ciocni polii analizorului si se vor pierde din fascicul.
4. Detectorul de ioni (Colectorul)
Ionii cu aceeasi valoare m/z formeaza in colector un curent slab. Acest curent este trimis spre amplificator.
5. Amplificatorul si inregistratorul
Dupa amplificare, curentul ionic este inregistrat in functie de m/z. Pentru inregistrarea unui spectru de masa, un spectrometru trebuie sa aiba un raspuns rapid, sa fie capabil sa inregistreze cateva sute de linii pe secunda si sa poata inregistra intensitati ale liniilor variind cu un factor mai mare de 103.
Conditia pentru ca un spectrometru de masa sa fie util este ca acesta sa poata face distinctia intre mase diferind cu o unitate. Astfel, pentru a selecta formulele moleculare posibile, liniile adiacente trebuie sa fie suficient de separate intre ele (Fig. 3.1).
Pentru determinarea rezolutiei spectrometrului de masa se considera doua linii adiacente din spectru (vezi Fig. 3.1), adica de aproximativ aceeasi masa (respectiv raport m/z). Puterea de rezolutie (R) a spectrometrului se defineste prin:
![]()
unde M1, M2 reprezinta masele ionilor moleculari.
Alaturi de puterea de rezolutie R un factor important este dat de raportul h/H ce caracterizeaza gradul de separare a picurilor celor doua semnale (vezi Fig. 3.1 a, b).
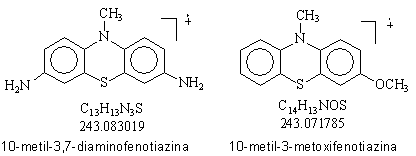
De exemplu pentru separarea maselor ionilor moleculari ai 10-metil-3,7-diaminofenotiazinei si 10-metil-3-metoxifenotiazinei este necesara o
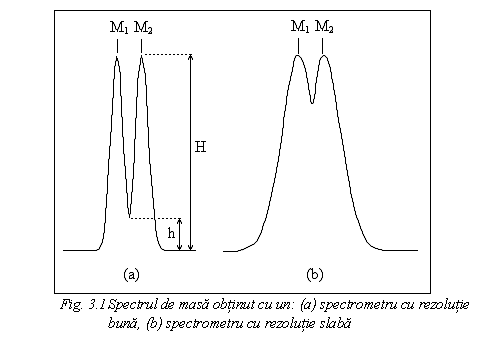
putere de rezolutie de 1:21.637, putere ce se poate
atinge numai cu spectrometre de masa cu dubla focalizare.
3.4. PREZENTARE GENERALA A UNUI SPECTRU DE MASA
Pentru interpretarea spectrelor de masa este necesar sa se elucideze urmatoarele aspecte:
(a) Identificarea ionului molecular
(b) Identificarea ionilor si proceselor de fragmentare caracteristice
(d) Reconstructia structurii moleculei pe baza mecanismelor de fragmentare standard.
Spectrele de masa sunt spectre de linii; aceasta inseamna ca semnalul generat de un ion apare sub forma unei linii. Aceste linii se mai numesc si picuri (de la "peak" care in limba engleza inseamna varf). Un spectru de masa contine urmatoarele tipuri de semnale:
-Linia ionului molecular
-Linii izotopice
-Linia de baza
-Linii generate p 727c21h rin fragmentarea ionului molecular (picuri de fragmentare).
Daca o molecula contine doar atomi formati dintr-un
singur izotop de abundenta naturala de 100%, linia de la valoarea m/z cea mai
mare (vezi figura 3.2.),
corespunde ionului molecular ![]() .
Majoritatea atomilor au mai multi izotopi, ceea ce determina aparitia de linii
la valori mai mari decat cea corespunzatoare ionului molecular
.
Majoritatea atomilor au mai multi izotopi, ceea ce determina aparitia de linii
la valori mai mari decat cea corespunzatoare ionului molecular ![]() .
Aceste linii se numesc linii izotopice sau picuri izotopice.
.
Aceste linii se numesc linii izotopice sau picuri izotopice.
Cel mai inalt pic din spectrul de masa se numeste pic de baza (sau linie de baza) si
corespunde ionilor cu viata lunga, care ajung la detector in cea mai mare
cantitate. Acesta poate fi identic cu picul molecular sau poate fi un pic
generat prin fragmentarea ionului
molecular ![]() .
Intensitatea procentuala relativa I%
se considera de 100% pentru picul de baza, iar intensitatile relative a
celorlalte picuri se determina in raport cu picul de baza. Cunoasterea
intensitatii procentuale relative permite cunoasterea abundentei procentuale relative pentru fiecare specie de ioni din
spectrul de masa.
.
Intensitatea procentuala relativa I%
se considera de 100% pentru picul de baza, iar intensitatile relative a
celorlalte picuri se determina in raport cu picul de baza. Cunoasterea
intensitatii procentuale relative permite cunoasterea abundentei procentuale relative pentru fiecare specie de ioni din
spectrul de masa.

Fig. 3.2 Tipuri de linii in spectrul de masa al unui compus organic
Pe langa linia ionului molecular, si a liniilor izotopice spectrul de masa mai contine si alte linii datorate ionilor (cationi sau radicali cationici) de fragmentare. Fragmentarea ionului molecular in spectrul de masa se face dupa anumite reguli specifice fiecarei clase de compusi.
Daca un ion (M1) se fragmenteaza dupa accelerare, inainte de a patrunde in campul magnetic, atunci in campul magnetic va fi deviata o particula de alta masa (M2). Curentului ionic rezultat ii va corespunde in spectrul de masa un semnal de intensitate mica, larg, cu masa aparenta M*:
![]()
Acest semnal este un asa numit semnal al unui ion metastabil. Masurarea masei ionului metastabil permite aflarea informatiei legate de obtinerea directa a M2 din M1 prin pierderea unui fragment neutru.
LINIILE IZOTOPICE
Atomii componenti ai unei molecule pot fi clasificati in trei categorii in functie de numarul si abundenta izotopilor pe care ii prezinta:
- Atomi monoizotopici: 19F, 31P, 127I;
- Atomi ce au un izotop foarte abundent: 1H, 12C, 14N, 16O:
- Atomi ce au doi izotopi abundenti: 35Cl, 37Cl, 79Br, 81Br
In Tabelul 3.1 sunt prezentate numerele de masa si abundentele izotopice relative pentru cateva elemente chimice.
Calcularea intensitatii relative a liniilor izotopice se realizeaza tinand cont de abundentele izotopilor atomilor din molecula.
Datorita faptului ca abundenta relativa a izotopului 13C este ≈1%, rezulta ca o molecula cu un atom de carbon va prezenta un pic izotopic M+1
de intensitate ~1% din cea a picului molecular M+. (Atentie! Procentul se refera la intensitatea M+. si nu la intensitatea picului de baza utilizat pentru calibrarea celorlalte picuri). Daca sunt n atomi de carbon, probabilitatea de a gasi un ion continand 13C este de n ori mai mare.
De exemplu, pentru un ion care contine n atomi de carbon exista o probabilitate de 1,1n % ca acel atom sa fie 13C si va conduce la o masa cu o unitate mai mare decat cea a ionului care contine doar atomi de 12C. De aici rezulta ca:
![]()
informatie foarte pretioasa, chiar daca are un caracter aproximativ.
Tabel 3.1. Numarul de masa, masa atomica, masa atomica relativa si abundenta izotopica relativa pentru cateva elemente chimice.
|
Atom |
Nr. de masa |
Masa atomica |
Masa atomica relativa |
Abundenta izotopica relativa |
|
H | ||||
|
He | ||||
|
B | ||||
|
Ga | ||||
|
C | ||||
|
Si | ||||
|
Ge | ||||
|
P | ||||
|
N | ||||
|
As | ||||
|
O | ||||
|
S | ||||
|
F | ||||
|
Cl | ||||
|
Br | ||||
|
I |
Astfel, in structura benzaldehidei, atomul de carbon are
doi izotopi principali, 12C (abundenta naturala 98,9 %) si 13C
(abundenta naturala 1,10 %), atomul de hidrogenul are izotopii 1H
(abundenta naturala 99,985 %) si 2H (abundenta naturala 0,015%), iar
oxigenul are izotopii 16O (abundenta naturala 99,76 %), 17O
(abundenta naturala 0,038 %) si 18O (abundenta naturala 0,20 %).
Astfel, linia de la m/z 106,12 corespunde sumei maselor ionilor cei mai
abundenti (12C71H616O)
si este cea a ionului molecular ![]() .
Liniile de la M+1 si M+2 sunt linii
izotopice, in care un atom sau doi atomi sunt inlocuiti cu izotopi cu masa
mai mare. Cu cat abundenta naturala a izotopilor elementelor ce compun compusul
organic este mai mare cu atat liniile izotopice sunt mai intense.
.
Liniile de la M+1 si M+2 sunt linii
izotopice, in care un atom sau doi atomi sunt inlocuiti cu izotopi cu masa
mai mare. Cu cat abundenta naturala a izotopilor elementelor ce compun compusul
organic este mai mare cu atat liniile izotopice sunt mai intense.
Pentru fiecare element intr-un ion dat, contributiile relative la liniile M+1 si M+2 sunt termenii dezvoltarii in serie a polinomului (p+q)n.
De exemplu, in cazul clorului exista doi izotopi 35Cl si 37Cl. Pentru ionii care contin un singur atom de clor, intensitatile relative ale liniilor, separate prin doua unitati de masa, sunt 3:1. Pentru un ion care contine 3 atomi de clor, dezvoltarea in serie a polinomului este p3+3p2q+3pq2+q3. Spectrul contine 4 linii. Primei linii ii corespunde ionul cu 3 atomi 35Cl, iar fiecare linie succesiva are un 35Cl inlocuit cu 37Cl, pana cand ultima linie corespunde ionului continand numai atomi 37Cl. Valorile m/z sunt separate
prin doua unitati, la M, M+2, M+4 si M+6. Deoarece abundentele relative ale 35Cl si 37Cl sunt 3:1 (p = 3, q = 1), intensitatile celor patru linii (neglijand contributia altor elemente) sunt p3 = 27, 3p2q = 27, 3pq2 = 9, q3 = 1, adica 27:27:9:1.
In cazul bromului, cei doi izotopi de 79Br si 81Br au abundente izotopice foarte apropiate, 50.54 % respectiv 49.46 %. Daca un ion contine doi atomi de brom atunci in spectrul de masa apar linii la M, M+2 si M+4, cu intensitatile relative 1:2:1, in timp ce pentru trei atomi se obtin linii la M, M+2, M+4 si M+6, de intensitati relative 1:3:3:1.
Daca un compus contine atat atomi de brom cat si de clor, atunci efectele lor sunt aditive. In figura 3.3. sunt prezentate cateva combinatii de astfel de atomi si liniile M+1 - M+4 intalnite de obicei in compusii organici.
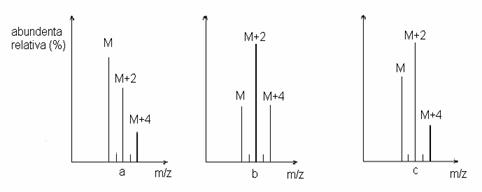 FFig. 3.3 Regiunea liniilor ionului molecular pentru un
compus care contine (a) doi
FFig. 3.3 Regiunea liniilor ionului molecular pentru un
compus care contine (a) doi
atomi de clor, (b) doi atomi de brom, (c) un atom de clor si un atom de brom.
Pentru doi atomi de clor si doi de brom prezenti in aceeasi molecula se obtin urmatoarele linii:
- pentru cei doi atomi de clor: p = 3, q = 1, (p+q)2 = 9 + 6 + 1, deci intensitatile liniilor sunt 9:6:1;
- pentru cei doi atomi de brom: p = 1, q = 1, (p+q)2 = 1+ 2 + 1, deci intensitatile liniilor sunt 1:2:1;
Combinand cele doua seturi de linii se obtine:
(9 : 6 : 1)x1 = 9 : 6 : 1
(9 : 6 : 1)x2 = 18 : 12 : 2
![]()
(9
: 6 : 1)x1 = 9
: 6 : 1
9 : 24 : 22 : 8 : 1
Spectrul contine 5 linii la M, M+2, M+4, M+6 si respectiv M+8, de intensitati relative 9 : 24 : 22 : 8 : 1.
In moleculele organice continand clor sau brom, liniile satelit de la M+1 si M+3 se datoreaza izotopului 13C. Prin conventie, termenul de ion molecular este atribuit ionului generat prin ionizarea moleculei continand izotopii cu masa cea mai mica.
DETERMINAREA FORMULEI MOLECULARE
Formula moleculara a unui compus sau a unui fragment poate fi adeseori determinata din masuratori de masa suficient de precise. Acest lucru este posibil datorita faptului ca masele atomice nu sunt numere intregi. De exemplu, cele patru molecule din Tabelul 3.2. au o masa nominala de 70 dar se poate face distinctie intre ele pe baza maselor exacte. Pentru masurarea greutatii moleculare exacte este necesar un spectrometru de masa cu o putere de rezolutie buna (de ex. in cazul primelor doua molecule diferenta de masa este 0,011234um iar puterea de rezolutie necesara R = 6231).
Tabelul 3.2. Formule moleculare corespunzatoare aceleiasi mase nominale.
|
Formula moleculara |
Greutatea moleculara |
|
C2H2N2O | |
|
C3H2O2 | |
|
C3H6N2 | |
|
C4H6O |
Utilizarea Liniilor M+1, M+2 in stabilirea formulei moleculare
In principiu, intensitatile liniilor M+1 si M+2 pot fi utilizate pentru obtinerea formulei moleculare. In practica, intensitatile liniilor M+1 si M+2 sunt in mod frecvent inexacte, adeseori mai mari decat se asteapta datorita reactiilor ionului molecular. De asemenea, pentru mase mai mari de 250, intensitatile liniilor M+1 si M+2 nu pot fi utilizate pentru diferentierea formulelor posibile fiind necesara utilizarea unor spectrometre de inalta rezolutie.
Exista cazuri speciale in care spectrometrele de masa de rezolutie scazuta pot fi utilizate pentru obtinerea de informatii privind formula moleculara. Prezenta atomilor de S, Si, Cl sau Br este usor detectabila prin contributia importanta la linia M+2. Prezenta atomilor de I, F si P monoizotopici poate fi detectata din aparitia unei linii M+1 suspect de mici in raport cu linia ionului molecular.
In mod general intensitatea liniei M + 1 se calculeaza cu formula:
I(M+1)= ![]()
Unde: ni este numarul atomilor de tip i,
ci este abundenta izotopica relativa a izotopului care determina aparitia liniei (m + 1) fata de izotopul cel mai abundent.
Daca molecula contine doar atomi de C, H, N, O, F, P, I, intensitatile aproximative ale liniilor M+1 si M+2 pot fi calculate cu formulele:
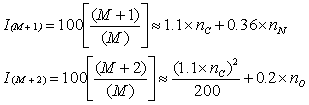
unde nC, nN si nO sunt numarul atomilor de carbon, azot, respectiv oxigen. Aceste ecuatii sunt utile in cazul in care exista o idee despre formula moleculara a compusului.
In cazul in care din spectrul de masa se cunoaste masa nominala, intensitatea picurilor IM+1, IM+2 si raportul acestora IM+1/IM+2 cu ajutorul tabelelor lui Beynon se pot determina formulele brute pentru moleculele ce corespund aceleiasi mase nominale. Dintre acestea se selecteaza formula bruta pentru care corespund valorile lui IM+1, IM+2 si IM+1/IM+2.
De exemplu, daca pe baza spectrului de masa se determina greutatea ionului molecular m/z=111, intensitatea picurilor IM+1=5,9%, respectiv IM+2=0,5% (ca % din inaltimea picului Im), si raportul IM+1/IM+2=10,8, din tabelul lui Beynon se gaseste formula bruta C5H5NO2 care corespunde acestor caracteristici.
IDENTIFICAREA IONULUI MOLECULAR
In cazul spectrometriei de masa clasice (in care moleculele aflate in stare de vapori sunt bombardate cu un fascicul electronic de inalta energie) ionul molecular poate sa lipseasca sau sa aiba o intensitate foarte mica.
Pentru cei mai multi ioni necunoscuti, clusterul ionic care apare la valori m/z mai mari este de asteptat sa-l reprezinte ionul molecular cu liniile M+1 adiacente, dar trebuie aplicate o serie de teste pentru confirmare.
In functie de intensitatea ionului molecular putem face o clasificare a diverselor clase de compusi astfel:
a). Ioni moleculari intensi prezinta in general hidrocarburile aromatice simple sau condensate, aril-alchileterii, fenolii, derivatii clorurati aromatici, aminele si nitroderivatii aromatici, alchinele, alchenele conjugate, derivatii heterociclici, etc. In aceste cazuri identificarea ionului molecular nu prezinta probleme deosebite.
b). Ioni moleculari mai putin intensi prezinta bromurile si iodurile de aril, arilcetonele, aldehidele, compusii ce pot genera prin fragmentare cation benzil.
c). Absenta ionilor moleculari sau prezenta unei linii M extrem de mici este caracteristica moleculelor puternic ramificate, indiferent de clasa functionala. Alcoolii si moleculele cu lanturi alchil lungi se fragmenteaza de asemenea usor si conduc la linii M foarte slabe. In acest caz identificarea picului caracteristic ionului molecular este dificila, elucidarea problemei presupune cunoasterea urmatoarelor reguli:
Abundentele izotopice Izotopul mai abundent determina aparitia liniei ionului molecular. Ceilalti izotopi contribuie la liniile M+1, M+2.
Regula azotului Daca molecula contine numai C, H, O, S, atomi de halogen sau un numar par de atomi de azot atunci ionul molecular are masa nominala para. Daca molecula contine un numar impar de atomi de azot atunci masa nominala a ionului molecular este impara.
In cazul ionilor de fragmentare regula azotului stipuleaza urmatoarele: cu exceptia ionilor ce contin un numar impar de atomi de azot toti ionii ce numar impar de electroni au masa para, iar cei cu numar par de electroni au masa impara.
Un corolar util spune ca fragmentarea moleculei in zonele in care exista legaturi simple conduce la fragmente ionice cu masa impara, daca ionul molecular are masa para si la fragmente ionice cu masa para, daca ionul molecular are masa impara. Pentru ca acest corolar sa fie valabil, fragmentul ionic trebuie sa contina toti atomii de azot ai moleculei (in cazul in care exista).
Fragmente ionice neobisnuite. Liniile observate la M-1, M-2, M-3 intr-un spectru de masa se atribuie de obicei pierderii succesive a atomilor de hidrogen, deoarece nu exista nici o grupare organica prin eliminarea careia sa se genereze direct picul M-3. Picurile a caror masa este cuprina in intervalul deschis (M-3; M-14) si intervalul inchis [M-21; M-25] nu pot fi atribuite unor atomi sau grupe de atomi din structura substantelor organice.
De asemenea, aparitia unei linii la M-14 (corespunzand pierderii directe a unui fragment CH2) este extrem de rara. De remarcat faptul ca daca molecula contine fluor, pot sa apara linii la M-19 (M-F) si M-20 (M-HF).
In concluzie prezenta unor linii intense in regiunile (M-3, M-14) sau [M-21, M-25] indica faptul ca:
(a) linia M nu corespunde ionului molecular sau,
(b) proba investigata nu este pura
DETERMINAREA NESATURARII ECHIVALENTE (NE)
In cazul unei substante necunoscute dupa determinarea formulei moleculare (cu ajutorul spectrului de masa) se incearca stabilirea unei formule structurale. Primul pas ce trebuie facut este determinarea nesaturarii echivalente a moleculei, aceasta fiind functie de tipul legaturilor chimice existente in compus.
Nesaturarea echivalenta (NE) este data de numarul perechilor de atomi de hidrogen care lipsesc din molecula astfel incat aceasta sa fie complet saturata. Prezenta unui ciclu, sau a unei duble legaturi, este echivalentul lipsei a doi atomi de hidrogen din molecula in acest caz NE fiind 1. O legatura tripla este echivalentul lipsei a patru atomi de hidrogen din molecula in acest caz NE fiind 2.
Cum intr-o molecula pot sa existe concomitent cicluri, legaturi duble sau triple nesaturarea echivalenta este o suma a acestora.
In cazul in care molecula contine numai atomi de carbon (nC), hidrogen (nH), azot (nN), halogen (nX), oxigen (nO) sau sulf (nS), NE este:
![]()
Atentie in determinarea nesaturarii echivalente nu se tine cont de numarul atomilor divalenti (de oxigen sau de sulf).
Formula de calcul a gradului de nesaturare, pentru o molecula de tipul AaBbDdEe, poate fi redata in forma generala astfel:
![]()
unde:
A este orice atom monovalent (H, D sau halogen)
B este orice atom bivalent (O, S.)
D este N, P sau orice atom trivalent (N, P.)
E este orice atom tetravalent (C, Si.)
a e reprezinta numarul atomilor mono, di-, tri- si tetravalenti din molecula.
Pentru o formula moleculara si o NE data se pot scrie mai multe formule structurale. Alegerea formulei structurale corecte se realizeaza in acord cu fragmentele ionice prezente in spectru de masa.
Trebuie insa sa atragem atentia asupra faptului ca o atribuire structurala, corecta si completa, nu se poate realiza numai pe baza spectrului de masa, fiind necesar ca substanta necunoscuta sa fie investigata si prin FTIR, RMN si difractie de raze X pe monocristal (daca metodele anterioare nu sunt concludente).
3.5. PROCESE DE FRAGMENTARE
3.5.1. REPREZENTAREA PROCESELOR DE FRAGMENTARE
Moleculele pot pierde dupa ionizare diverse tipuri de radicali sau fragmente neutre; de exemplu, un alcan cu structura neramificata se fragmenteaza cu formarea unui radical metil si a unui cation conform schemei:
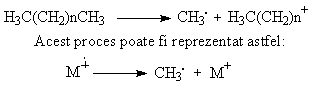
Eliminarea radicalului metil se reprezinta sub o forma mult simplificata astfel: M-15 sau M-CH3 (unde M reprezinta ionul molecular iar 15 este masa radicalului metil). Aceasta reprezentare este valabila si pentru alte fragmente; de exemplu pierderea unei molecule de etena se poate reprezenta astfel: M-28 sau (M-C2H4). Alte exemple sunt prezentate in tabelul 3.3.
Tabel 3.3. Reprezentarea unor fragmente ionice generate de eliminarea unor molecule simple sau radicali
|
Fragmentul eliminat |
Mod de reprezentare |
Fragmentul eliminat |
Mod de reprezentare |
|
H· |
M-1 |
NO· |
M-30 |
|
CH3· |
M-15 |
CH3O· |
M-31 |
|
HO· |
M-17 |
Cl· |
M-35 |
|
H2O |
M-18 |
H3CCO . |
M-43 |
|
CN· |
M-26 |
Br | |
|
HCN |
M-27 |
H5C6CH2· |
M-91 |
|
H2C=CH2, CO |
M-28 |
I |
M-127 |
|
HCO· |
M-29 |
Prin aceste notatii se intelege ca fragmentul poate fi
atat cu numar par de electroni, de exemplu (M-15)+, cat si cu numar
impar de electroni, de exemplu, ![]() .
.
3.5.2. REGULI SI TIPURI DE FRAGMENTARI
Fragmentarea ionilor moleculari in spectrometrul de masa se face specific fiecarei clase de substante. Vom prezenta in continuare cateva reguli de fragmentare.
a) Ruperea legaturilor σ in alcani:
In cazul alcanilor, ionii moleculari au sarcina pozitiva nelocalizata iar fragmentarea se poate realiza prin:
- Ruperea oricarei legaturi σ C-C, cu formarea de cationi si radicali in cazul normal alcanilor.
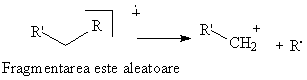
- In cazul moleculelor ramificate fragmentarea se face preferential cu ruperea legaturilor C-C de la atomul de carbon cuaternar sau tertiar.
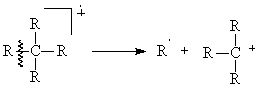
Aceasta este o consecinta a stabilitatii ridicate a carbocationilor tertiari in raport cu cei secundari, care la randul lor sunt mai stabili decat cei primari. In general, cel mai mare substituent al unei ramuri este eliminat mai rapid ca radical, probabil datorita faptului ca radicalii liniari lungi pot deveni mai stabili prin delocalizarea electronului neimperecheat.
b). Scindarea α "oniu"
Acest proces apare la fragmetarea moleculelor in care exista heteroatomi (alcooli, amine, eteri, tioeteri, cetone). Ionizarea moleculei are loc (cel mai probabil) prin pierderea unui electron de la heteroatom, proces urmat de scindarea legaturii σ C-C din pozitia β fata de acesta, sarcina ramanand la fragmentul ce contine heteroatomul. Stabilizarea cationului rezultat se realizeaza prin conjugare cu electronii neparticipanti de la heteroatom, cu formarea unui ion oxoniu, amoniu, sulfoniu, etc.
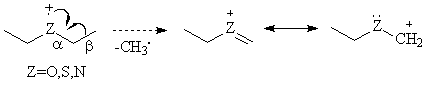
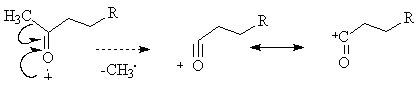
In cazul in care gruparile R, R' sunt radicali alchil scindarea legaturii din pozitia β se face preponderent cu formarea radicalului cu catena cea mai lunga.
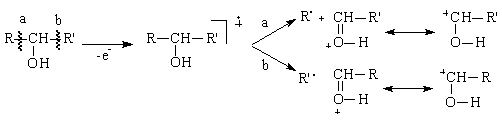
c) Eliminarea unor molecule neutre prin ruperea unor legaturi σ
Ruperea mai multor legaturi σ conduce la eliminarea unei molecule neutre, (de ex. CO, SO2 , HCN, HCl, H2O, C2H4, C2H2). Procesul de eliminare poate fi acompaniat de procese de transpozitie a unor atomi sau grupari functionale.
In spectrul de masa al fenolului se remarca prezenta ionilor de fragmentare de tip M-28 caracteristici pierderii unei molecule de monoxid de carbon. Fragmentarea se realizeaza prin migrarea unui atom de hidrogen de la heteroatom la ciclu urmata de eliminarea monoxidului de carbon.
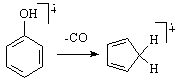
In spectrul de masa al benzensulfonamidei se remarca prezenta unei linii la valoarea M-64, generat prin eliminarea unei molecule de SO2, concomitent cu transpozitia gruparii NH2.
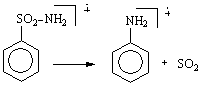
Eliminarea unor fragmente neutre se poate realiza si din ionii de fragmentare, nu numai din ionul molecular, un exemplu in acest sens fiind eliminarea succesiva a doua molecule de acetilena din ionul tropiliu(m/z 91).

Aparitia in spectru a succesiunii de fragmente 91-65-39 denota prezenta in molecula a unui fragment benzil C6H5-CH2-
Ciclohexena se fragmenteaza printr-un mecanism de tip retro-Diels-Alder, cu formarea unei molecule neutre de etena si a unui radical cation butadienil stabilizat prin conjugare.
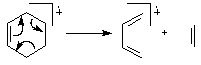
Fragmentare retro Diels-Alder
d) Transpozitii
Procesele de fragmentare a ionului molecular sau a altor ioni generati din ionul molecular ce decurg cu migrarea unor atomi sau grupari sunt destul de obisnuite. Un exemplu de transpozitie intalnita la diverse clase de compusi ce contin o legatura multipla dubla sau tripla, omogena sau heterogena, este transpozitia McLafferty. F.W. McLafferty a pus in evidenta migrarea unui atom de hidrogen, situat la atomul din pozitia γ fata de legatura multipla, la atomul terminal al dublei legaturi, printr-o stare de tranzitie hexaatomica.
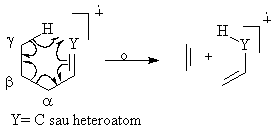
Astfel de transpozitii se intalnesc la cetone, aldehide, olefine, acizi carboxilici, amide, esteri, nitrili, alchilbenzeni si decurg cu eliminarea unor molecule neutre.
e) Fragmentarea alilica
Legaturile duble favorizeaza scindarea alilica (scindarea legaturii C-C din pozitia β fata de legatura dubla) care conduce la carbocationi alilici stabilizati prin rezonanta.
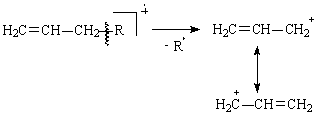
f) Ciclurile saturate pierd gruparile alchil legate de ciclu. Sarcina pozitiva tinde sa ramana pe fragmentul ciclic.
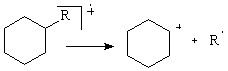
g) Fragmentarea β aromatica
In compusii aromatici substituiti cu grupari alchil, ruperea are loc la nivelul legaturii β din gruparea alchil, cu formarea ionului benzil C7H7+ m/e=91. Deoarece in acest ion toti cei sapte atomi de hidrogen sunt echivalenti se accepta rearanjarea acestuia sub forma de ion tropiliu. Ionul tropiliu prezinta stabilitate ridicata, si este caracteristic compusilor organici in structura carora se afla o grupare benzil.

h) Regula numarului impar de electroni
Aceasta regula se refera la faptul ca un ion cu un numar par de electroni nu va fragmenta in mod obisnuit in doua specii cu numar impar de electroni, cu alte cuvinte el nu va conduce la un radical sau la un ion al unui radical, deoarece energia totala a acestui amestec de produsi ar fi prea mare. Exista insa si exceptii de la aceasta regula:
![]() A+
A+ ![]()
Par impar impar
Calea cea mai frecventa de degradare este la un alt ion si la o molecula neutra.
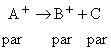
Ionii radicalilor, fiind specii cu numar impar de electroni, pot elimina o molecula neutra, ramanand un alt ion al unui radical:

Ionii radicalilor pot de asemenea sa se degradeze la un radical si la un ion:
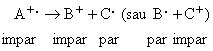
i) Intensitatea ionului molecular:
Exista o serie de reguli care ne permit sa aproximam intensitatea ionului molecular in cadrul unor clase de substante:
- In cadrul aceleiasi clase amplitudinea relativa a liniei ionului molecular este mai mare pentru compusii care sunt formati dintr-un lant liniar comparativ cu cei ramificati si descreste odata cu cresterea gradului de ramificare.
- Amplitudinea relativa a liniei ionului molecular scade, de obicei, cu cresterea masei moleculare in seria omoloaga. Esterii mari sunt exceptii de la aceasta regula.
- Legaturile duble, structurile ciclice si in special ciclurile aromatice sau heteroaromatice stabilizeaza ionul molecular si astfel creste probabilitatea aparitiei lui.
3.6. SPECTRE DE MASA ALE PRINCIPALELOR CLASE DE COMPUSI ORGANICI.
In cazul in care se cunoaste formula moleculara a compusului investigat se pot prezice anumite fragmentari ce urmeaza a avea loc, fragmentari specifice clasei de compusi din care substanta investigata face parte.
3.6.1. HIDROCARBURI
3.6.1.1 Alcani
In cazul alcanilor intotdeauna linia ionului molecular este observabila, desi este cu atat mai putin intensa cu cat lungimea lantului molecular sau ramificarea acestuia este mai mare. Prin fragmentare, alcanii pierd succesiv grupari CH2, ceea ce determina aparitia in spectru a unor grupe de linii separate prin cate 14 unitati de masa. Linia cea mai intensa din fiecare grup corespunde unui fragment CnH2n+1 si apare la m/z 14n+1. Aceasta este insotita de linii ale fragmentelor CnH2n si CnH2n-1. Cele mai abundente fragmente sunt cele cu 3 si 4 atomi de carbon iar abundentele celorlalte fragmente descresc de-a lungul unei curbe netede pentru mai mult de 5 atomi de carbon. Linia M-CH3 este in general foarte mica sau lipseste din spectru. Alcanii care contin mai mult de 8 atomi de carbon prezinta spectre aproape similare, identificarea compusului facandu-se atunci cu ajutorul liniei ionului molecular.
In spectrul de masa al n-dodecanului: CH3(CH2)10CH3 ionul molecular apare la m/z 170 dar abundenta relativa a acestuia este de aproximativ 5%. Picul de baza (abundenta relativa 100%) este cel de la m/z=57 corespunzator fragmentului C4H9+. Alte fragmente importante prezente in spectru sunt:
- la m/z=43 corespunzator ionului C3H7+ (81%),
- la m/z=71 corespunzator ionului C5H11+ (50%),
- la m/z=85 corespunzator ionului C6H13+ (30%),
- la m/z=41 corespunzator ionului C3H5+ (22%),
- la m/z=29 corespunzator ionului C2H5+ (18%),
- la m/z=27 corespunzator ionului C2H3+ (8%),
Pe langa liniile ionilor CnH2n+1 intre C2 si C5 se observa ionii alchenil CnH2n-1 (la m/z 27 (C2H3+), 41(C3H5+), 55, 69) formati prin pierderea a doi atomi de hidrogen si ionii CnH2n. Ionii alchil pot elimina o molecula de mici dimensiuni, rezultand ioni metastabili cu linii de intensitate foarte mica: de exemplu ionii C2H5+ si C3H7+ elimina o molecula de hidrogen, generand ionii C2H3+, respectiv C3H5+. Ionul C4H9+ elimina o molecula CH4 generand ionul C3H5+.
Spectrele hidrocarburilor saturate ramificate sunt asemanatoare cu cele ale hidrocarburilor liniare, cu deosebirea ca descresterea uniforma a intensitatilor grupurilor de linii este intrerupta de fragmentarea preferentiala la nivelul fiecarei ramificatii. Fragmentarea compusului in dreptul ramificatiei conduce de obicei la expulzarea unui radical si la retinerea sarcinii pozitive pe atomul de carbon substituit. De asemenea, se manifesta preferinta pentru formarea de cationi tertiari, mai mult decat a celor secundari sau primari.
In Schema 3.2 sunt reprezentate fragmentarile ce au loc in spectrul de masa al 5-metilpentadecanului. Picurile de la m/z 169 si 85 corespund fragmentarii ionului molecular pe calea a respectiv b. Abundenta relativa a ionilor C6H13+ este considerabil mai mare decat a ionilor C12H25+, respectiv C15H31+, aceasta fiind in acord cu regula de fragmentare care stipuleaza ca favorabila eliminarea radicalilor alchil cu catena cea mai mare. Linia de la M-15 este un indiciu suplimentar al prezentei gruparii metil.
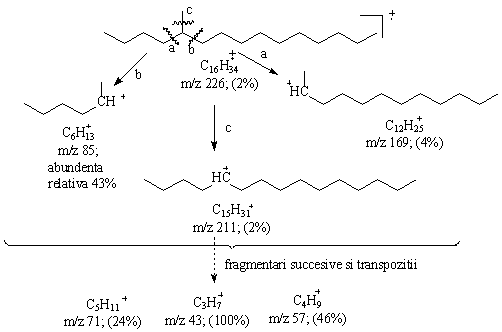
Procesul de fragmentare a ionului molecular atat la alcanii ramificati cat si la cei neramificati este insotit de transpozitii aleatorii cu formare de cationi stabili; asa se explica prezenta in spectru a fragmentelor de la m/z 43, 57, 71 a caror abundenta relativa este considerabil mai mare decat a fragmentelor generate direct din ionul molecular.
3.6.1.2 Cicloalcani
Cicloalcanii prezinta de obicei fragmentari complexe, influentate de dimensiunea ciclului acestora. Pentru cicloalcanii simpli, linia ionului molecular este usor observabila, intensitatea sa scazand odata cu cresterea ramificarii compusilor.
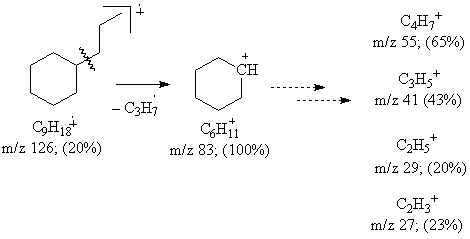
Schema 3.3
Cele mai uzuale fragmentari constau in pierderea unor radicali alchil sau alchenil din catena, sarcina pozitiva ramanand pe ciclu. In spectrul de masa al n-propilciclohexanului, (Schema 3.3), se poate observa fragmentarea ionului molecular cu eliminarea unui radical propil si formarea cationului ciclohexil, care este si pic de baza. Fragmentarile ulterioare ale cationului ciclohexil conduc la cationii C4H7+, C3H5+, C2H5+, C2H3+.
3.6.1.3 Alchene
In cazul alchenelor simple, linia ionului molecular este destul de bine rezolvata. Fragmentarea alchenelor presupune ruperea unei legaturi alilice (din pozitia b fata de legatura dubla) cu formarea unui cation alilic stabilizat prin rezonanta. Deoarece si radicalul si cationul alil sunt stabilizati prin conjugare, exista o competitie in formarea acestora.
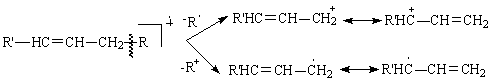
Localizarea legaturii duble in alchenele aciclice este dificila datorita posibilitatii de migrare a dublei legaturi in fragmentele formate. In alchenele ciclice (in special in cele policiclice), pozitia legaturii duble poate fi pusa in evidenta datorita scindarii alilice, in acest caz neexistand posibilitatea de migrarea a dublei legaturi.
-Mircenul, derivat din clasa terpenelor ce contine trei duble legaturi in molecula, prezinta in spectrul de masa cationi la m/z=69, 67, 93, generati prin fragmentarea in pozitia alilica si cationi m/z=55 si 41, generati prin fragmentari succesive insotite de transpozitii ale dublei legaturi. Picul de baza apare la m/z=41(100%). Fragmentul de la m/z=93 se formeaza in urma unei transpozitii a dublei legaturi in ionul molecular urmata de o scindare in pozitie alilica (Schema 3.4).
3.6.1.4 Alchine
In acest caz nu exista nici un mod tipic de fragmentare. Astfel, pentru 1-butina si 2-butina, linia ionului molecular este linie de baza, dar pentru alchine mai mari, linia ionului molecular este mai mica. Pierderea unui radical alchil conduce in multe cazuri la linii intense (la M-15, M-29,.) in timp ce eliminarea unei alchene conduce la linii la M-28, M-42.
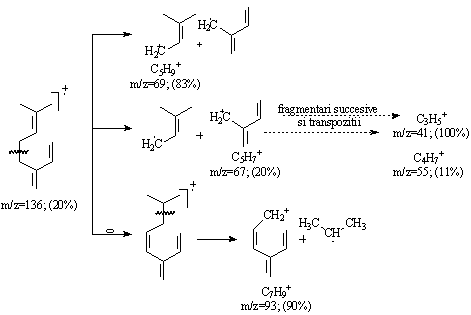
Schema 3.4
3.6.1.5 Hidrocarburi aromatice
Ionii moleculari ai hidrocarburilor aromatice nesubstituite sunt intotdeauna abundenti, si frecvent ionul molecular este si ion de baza, datorita stabilizarii prin conjugare a acestui ion.
In spectrul de masa al benzenului, picul molecular este si pic de baza si este insotit de picuri la M-1, M+1 de intensitate redusa. Alte picuri prezente sunt la M-26 m/z=52, generat prin pierderea unei molecule de acetilena si la m/z=39 un pic de intensitate redusa..
In spectrul de masa al naftalinei, (Schema 3.5), picul molecular este si pic de baza, fiind insotit de picuri la M-1 si M+1 cu o abundenta relativa de aproximativ 10 respectiv 11%.
In spectru mai sunt prezente picuri de intensitate redusa, sub 15%, la valori m/z=102; (8%), m/z=76 (6%), generat prin pierderea unei molecule de acetilena, precum si m/z=64 (11%), m/z=51 (12 %) si m/z=39 (4%).
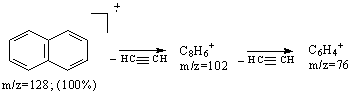
Schema 3.5
In cazul hidrocarburilor aromatice substituite cu catene alchil apare picul caracteristic la m/z=91, datorat ionului tropiliu C7H7+. Spectrul de masa al toluenului prezinta un ion molecular abundent dar are ca pic de baza cationul tropiliu la m/z=91. Un alt pic de intensitate redusa apare la m/z=65 generat prin eliminarea unei molecule de acetilena din ionul tropiliu, (Schema 3.6).

3.6.2. DERIVATI HALOGENATI
Spectrele de masa ale derivatilor halogenati sunt influentate de atomul de halogen atat in ce priveste modul de fragmentare cat si prin intensitatea si numarul de picuri izotopice ce insotesc picul molecular sau picurile de fragmentare, astfel:
- Compusii ce contin fluor si iod nu prezinta picuri izotopice.
- Compusii ce contin clor si brom prezinta picuri izotopice situate la M+2, M+4 a caror intensitate este functie de numarul atomilor de halogen din molecula.
- Derivatii halogenati alifatici ce contin fluor se fragmenteaza usor cu pierderea unei molecule de acid fluorhidric, si prezinta un pic intens la M-HF (M-20).
- Derivatii halogenati alifatici ce contin clor se fragmenteaza cu eliminare de acid clorhidric generand picuri la M-36 si M-38. Prezenta celor doua picuri este o consecinta a izotopilor de masa 35 si 37 ai clorului aflati in raport de 3:1. De asemenea in spectru pot fi observate si picuri pentru HCl+ la m/z 36 si 38. Pierderea atomului de clor Cl· determina aparitia unor picuri putin intense M-35 si M-37.
- Derivatii halogenati alifatici ce contin brom in molecula se fragmenteaza preferential cu eliminarea halogenului generand picuri intense la M-79 si M-81.
- Derivatii halogenati alifatici ce contin iod prezinta urmatoarele picuri caracteristice: m/z 127 pentru I+ si M-127 generat de eliminarea iodului.
Derivatii halogenati aromatici, in care atomul de halogen este grefat pe nucleu, prezinta linii intense ale ionilor moleculari. Fragmentarea este dictata de stabilitatea relativa a cationilor aril, halogenul fiind eliminat ca radical, dupa care urmeaza fragmentarea obisnuita a restului aromatic.
In spectrul de masa al bromometil benzenului apar doua picuri mici la m/z=170 si 172 de aproximativ aceeasi intensitate coerspunzatoare ionului molecular, aceasta fiind o dovada ca molecula contine brom (raportul intre izotopii 79Br si 81Br este de 1:1). Picul de baza este la m/z=91 si se datoreaza eliminarii de brom cu formarea cationului benzil care prin transpozitie genereaza ionul tropiliu (Schema 3.7). Un alt pic de intensitate redusa prezent in spectru este cel de la m/z=65 generat prin eliminarea unei molecule de acetilena din ionul tropiliu.

Schema 3.7
3.6.3 COMPUSI HIDROXILICI
3.6.3.1 Alcooli
In general in spectrele de masa ale alcoolilor primari si secundari prezinta picuri de intensitate redusa pentru ionii moleculari, iar in cazul alcoolilor tertiari picul corespunzator ionului molecular nu apare in spectru.
Sub impactul fluxului de electroni alcoolii sufera aceleasi tipuri de fragmentari, difera insa abundenta relativa a cationilor sau radical cationilor generati. Preferinta pentru anumite tipuri de fragmentari este functie de natura alcoolului: alifatic sau aromatic, primar, secundar, tertiar si nu in ultimul rand de lungimea catenei.
Pentru a ilustra preferinta de scindare a ionului molecular, in cazul alcoolilor alifatici, vom prezenta schemele de fragmentare a 3 izomeri ai pentanolului: 1-pentanol (alcool primar), 2-pentanol (alcool secundar), 2-metil-2-butanol (alcool tertiar), (Schema 3.8a-c). Cea mai importanta fragmentare pe care o sufera alcoolii este ruperea legaturii β fata de oxigen, cu formarea unui radical alchil si a unui cation stabilizat prin conjugare (scindare "α oniu") vezi calea a si a' din schemele 3.8a-c). In cazul in care atomul de carbon, de care este grefata gruparea hidroxi, este secundar sau tertiar, prin scindarea legaturilor din pozitia β fata de oxigen se formeaza doi radicali si doi cationi (calea a si a'' din schemele 3.8b-c), preferentiala fiind scindarea in care se formeaza radicalul alchil cu numar mai mare de atomi de carbon. De exemplu in cazul eliminarii unui radical metil din 2-metil-2-butanol (Schema 3.8c calea a,a'') se formeaza un cation cu o abundenta relativa de 52% in timp ce eliminarea unui radical propil conduce la formarea unui cation cu o abundenta relativa de 100%.
Un alt tip de fragmentare pentru alcooli alifatici este eliminarea unei molecule de apa (calea b din Schemele 3.8a-c). Prezenta picului de la M-H2O se poate datora si deshidratarii termice a alcoolilor, proces care decurge fara transpozitia hidrogenului g
Alcoolii cu mai mult de patru atomi de carbon pot elimina simultan o alchena si apa. In urma acestui proces, in spectrul de masa se observa un pic la M-(H2O+CnH2n) (calea c din Schemele 3.8a-c). In cazul 1-pentanolului pe aceasta cale este generat cationul cu abundenta relativa de 100% (pic de baza).

Schema 3.8c

Schema 3.8a

Schema 3.8b
3.6.3.2 Fenoli
Fenolii simpli prezinta linii intense ale ionilor moleculari. Cea mai frecventa scindare consta in pierderea unei molecule de monoxid de carbon cu formarea radical cationului m/z=66 urmata de eliminarea unui atom de hidrogen si formarea cationului ciclopentadienil m/z=65 (Schema 3.9).

Schema 3.9
Din spectrul de masa al o-etilfenolului se observa preferinta pentru eliminarea radicalului metil (Schema 3.10 calea a) si formarea unui cation ce prezinta un pic la m/z=107, (100%) comparativ cu eliminarea unui atom de hidrogen de la gruparea metilen grefata pe nucleul aromatic (Schema 3.10 calea b). Cationul cu m/z=107 sufera succesiv reactii de transpozitie si fragmentare cu eliminare de monoxid de carbon si hidrogen conducand la cationul fenil m/z=77.

Schema 3.10
3.6.4. ETERI
3.6.4.1 Eteri alifatici
Linia ionului molecular la eterii alifatici este putin intensa. In cadrul acestei clase de compusi, ionul molecular se fragmenteaza preponderent pe doua cai:
a). Scindarea "oniu" a legaturii σ C-C din pozitia β fata de oxigen cu eliminarea unui radical alchil si a unui cation stabilizat prin conjugare. Daca in cation exista hidrogen in pozitia β (fata de oxigen), acesta sufera o noua fragmentare cu eliminarea unei molecule neutre de alchena. Fragmentarea decurge cu transpozitia atomului de hidrogen β de la carbon la oxigen (Schema 3.11, calea a,a').
b). Ruperea legaturii C-O, cu formarea unor carbocationi alchil, (Schema 3.11, calea b,b').
In Schema 3.11 sunt prezentate principalele fragmente din spectrul de masa al etil-propil eterului.
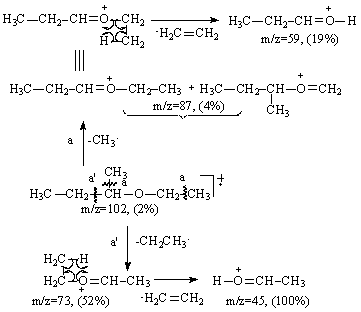
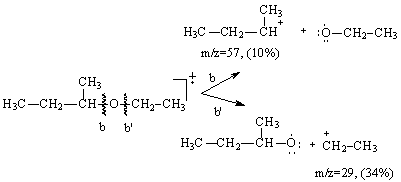
Schema 3.11
3.6.4.2 Alchil-aril eteri
Spre deosebire de eterii alifatici in acest caz picul molecular este pronuntat. Alchil-aril eterii se fragmenteaza astfel:
a). Eliminarea unei molecule neutre de alchena, proces insotit de transpozitia unui atom de hidrogen β (atom de hidrogen ce apartine unui atom de carbon dispus in β fata de oxigen). In ceea ce priveste transpozitia hidrogenului β aceasta se poate realiza prin stare de tranzitie de 4 respectiv 6 centri parerile in acest sens fiind impartite. In urma acestui proces se formeaza radicali cationi de masa m/z=94 (in cazul in care nucleul aromatic este nesubstituit) care sufera fragmentari succesive generand picuri la m/z=66 corespunzator radical cationului ciclopentadienei si m/z=65 pentru cationul ciclopentadienil, (Schema 3.12).
In cazul anisolului transpozitia hidrogenului β este insotita de eliminarea unei molecule de formaldehida si generarea cation radicalului C6H6+. la m/z=78. Acesta elimina un atom de hidrogen conducand la cationul fenil m/z=77, (Schema 3.13).
b). Scindarea legaturii oxigen-alchil (dispusa in β fata de nucleul aromatic) cu eliminarea unui radical alchil si formarea unui cation aril-oxi de masa m/z=93 care prin fragmentare genereaza cationul ciclopentadienil m/z=65, (Schema 3.14).
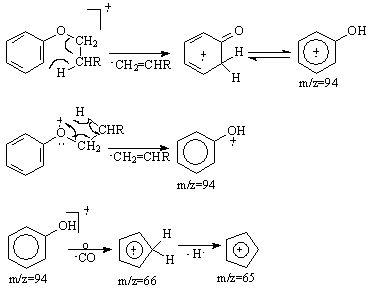
Schema 3.12
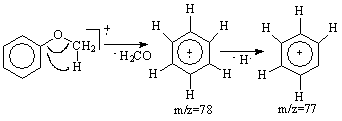
Schema 3.13
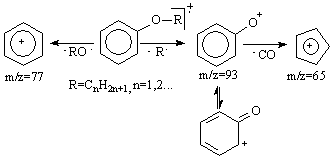
Schema 3.14
O alta posibilitate de fragmentare este scindarea legaturii oxigen-aril cu eliminarea unui radical RO . si a unui cation fenil m/z=77.
3.6.5 COMPUSI CARBONILICI
3.6.5.1 Aldehide
In spectrele de masa ale aldehidelor picul caracteristic ionului molecular M+. este putin intens (in cazul in care catena alchil este lunga), in timp ce pentru aldehidele aromatice este intens. Scindarea ionului molecular se poate face pe mai multe cai:
a). Eliminarea unui atom de hidrogen si formarea unui cation acil este specifica aldehidelor alifatice si aromatice. Picurile M-1 sunt insa mai intense in cazul aldehidelor aromatice datorita stabilitatii ridicate a cationului ArCO+, (Schema 3.15 calea a).
b) Ruperea legaturii C-C, adiacenta gruparii carbonil, cu eliminarea unui radical alchil R. si a cationului HCO+ cu masa m/z=29. In cazul aldehidelor alifatice superioare picul de la m/z 29 se datoreaza ionului C2H5+, (Schema 3.16 calea b).
c). Transpozitia Mc. Lafferty are loc in cazul aldehidelor cu hidrogen in pozitia g, si consta in migrarea hidrogenului g la oxigen si eliminarea unei molecule neutre de alchena si a unui cation radical (Schema 3.14 calea c)
d). In cazul aldehidelor alifatice, cu catene de carbon mari, apar picuri la M-18 (eliminarea apei), M-28 (eliminare etena), M-43 (pierderea gruparii CH2=CH-O+) si M-44 (pierderea gruparii CH2=CH-OH), (Schema 3.15 calea d).
In Schema 3.15 este prezentata fragmentarea nonan aldehidei. Se poate observa ca in cazul transpozitiei McLafferty sarcina pozitiva poate sa ramana la fragmentul ce contine heteroatomul (calea c) sau la radicalul alchil generand picul M-44 (calea c').
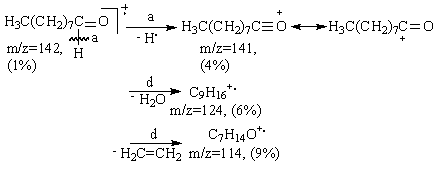
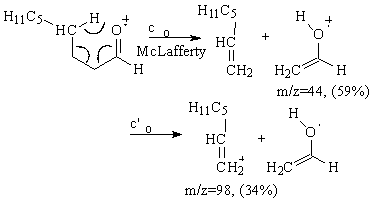
Schema 3.15
In cazul aldehidelor acetice, propionice si butirice o cale de fragmentare importanta este scindarea legaturii C-C adiacente gruparii carbonil cu formarea cationului H-C O+ cu m/z=29, care in cazul primelor doua este si pic de baza, (Schema 3.16).
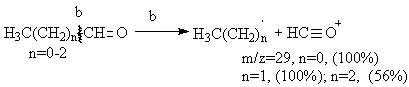
Schema 3.16
3.6.5.2 Cetone
In cazul cetonelor picul ionului molecular este in general intens. Principalele cai de fragmentare a ionului molecular sunt scindarea α (vezi aldehide) si transpozitia McLafferty.
a). Scindarea a este mai importanta in cazul cetonelor decat la aldehide, iar pentru metil respectiv aril-cetone aceasta scindare conduce la cationii: acetoniu CH3CO+ (m/z 43) si respectiv C6H5CO+ (m/z 105) care de obicei au abundenta maxima in spectru (Schema 3.17 calea a).
In cazul cetonelor alifatice in urma scindarii α, gruparea alchil se elimina preferential sub forma de radical, sarcina pozitiva ramanand la cationul acil [R-C=O]+. In cazul in care cetona alifatica este asimetrica se constata ca gruparea alchil mai mare se elimina preferential fata de gruparea alchil cu numar mai mic de atomi de carbon.
b). Transpozitia McLafferty are loc daca in molecula exista atomi de hidrogen γ atat in cazul aldehidelor cat si in cel al cetonelor. In cazul aldehidelor superioare ionul generat prin transpozitie McLafferty poate suferi o noua transpozitie cu eliminare de alchena (Schema 3.17 calea b) .
In Schema 3.17 sunt exemplificate scindarea α si transpozitia McLafferty in cazul octan-3-onei.
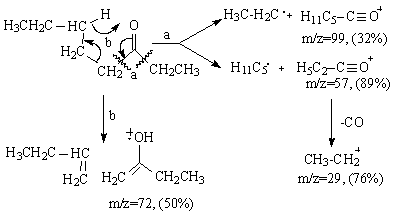
Schema 3.17
3.6.6. ACIZI CARBOXILICI SI DERIVATII ACESTORA
3.6.6.1 Acizi carboxilici
In cazul acizilor carboxilici fragmentarea ionului molecular se poate realiza pe mai multe cai in functie de natura acidului, alifatic sau aromatic, marimea catenei alchil sau natura substituentilor prezenti pe nucleul aromatic.
Acizii carboxilici alifatici se fragmenteaza prin:
a). transpozitie McLafferty daca exista hidrogen γ (Schema 3.18).
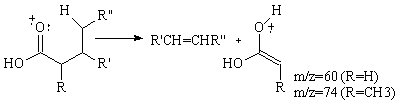
Schema 3.18
b). scindare a cu eliminarea radicalului alchil si formarea cationului COOH+ m/z=45. De asemenea este posibila si eliminarea radicalului hidroxi si a unui cation acil RC=O+.
c). Scindarea legaturii β C-C (fata de gruparea C=O) cu formarea unui cation de tip H2CCOOH+, cu m/z=59, putin abundent in spectru.
d). Scindarea legaturii γ C-C (fata de gruparea C=O) cu formarea unui cation de tip [H2C-CH2COOH]+, cu m/z=73. Dupa alti autori picul de la m/z=73 este dat de o dubla transpozitie a hidrogenului cu eliminarea unui radical RCH2CH2CH2. si a cationului H2C=CH2-C(=OH+)(OH), schema 3.19.
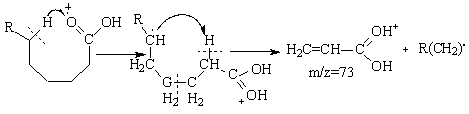
Schema 3.19
3.6.6.2 Esteri
Esterii alifatici prezinta in spectrele de masa picuri de intensitate redusa pentru ionul molecular. De asemenea se remarca prezenta in spectru a picurilor de tip M+1 si M+2, datorita unei reactii ion-molecula care apare in proba in cazul in care aceasta este utilizata in cantitate mare. Se utilizeaza cantitati relativ mari de proba pentru ca picul ionului molecular sa fie observabil. Fragmentarea ionului molecular se realizeaza in principal pe doua cai, scindare α si transpozitie McLafferty.
a). Scindarea α conduce la patru tipuri de ioni si se realizeaza prin ruperea legaturilor adiacente gruparii C=O. Abundenta relativa a celor patru tipuri de ioni (R+, RO-CO+, R-C O+, RO+) este functie de natura si marimea esterului (Schema 3.20 calea a,a').
b). Scindarea McLafferty in cazul metil esterilor decurge cu transpozitia unui proton γ din gruparea alchil la atomul de oxigen din gruparea C=O si eliminarea unei alchene (Schema 3.20 calea b).
In cazul esterilor proveniti din alcooli superiori sunt posibile mai multe tipuri de fragmentari insotite de transpozitie astfel:
b1. transpozitia unui proton β (din gruparea alchil ce a apartinut alcoolului) la atomul de oxigen din gruparea C=O cu eliminarea unui acid carboxilic si a unui radical cation alchenil.
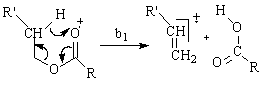
b2. transpozitia unui proton d (din gruparea alchil ce a apartinut alcoolului) la atomul de oxigen din gruparea eterica cu eliminare de acid, etena si a unui radical cation alchenil.
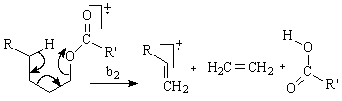
b3. transpozitia a doi atomi de hidrogen la atomii de oxigen din gruparea carboxil cu eliminarea unui radical alchenil si a unor cationi cu masa m/z= 61, 75, 89, etc. (pentru R= (CH2)nCH3 unde n=0, 1, 2.)

Schema 3.20 prezinta tipurile de fragmentari prezente in spectrul de masa al octanoatului de metil.
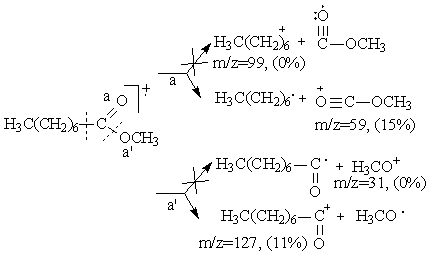
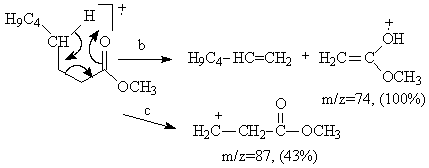
Schema 3.20
In cazul octanoatului de metil in spectrul de masa nu apar fragmente de masa m/z=99 si m/z=31, deci scindarea a nu decurge cu formarea cationilor heptenil si metoxi. De asemenea, in spectrul octanoatului de metil si a omologilor acestuia, este prezent un pic la m/z=87, (Schema 3.20 calea c) formal atribuit unei formule de tipul (CnH2n-1O2)+, [H2C-H2C-CO2CH3]+, a carei formare nu se explica prin fragmentarile mentionate anterior.
3.6.6.3 Amide
In functie de tipul amidei: alifatica, alifatica-aromatica, aromatica, primara, secundara sau tertiara si de marimea catenei, in spectrul de masa sunt prezente anumite fragmente caracteristice.
In cazul amidelor alifatice primare ionul molecular se poate fragmenta in principal prin: scindarea a, transpozitia McLafferty, eliminarea gruparii NH2., sau scindarea legaturii s dintre atomii Cg-Cd
a). Scindarea a in amidele alifatice primare, RCONH2, conduce
la radicalul alchil ![]() si cationul CONH2+ (m/z
44) care genereaza un pic intens in spectru (Schema 3.21 calea a).
si cationul CONH2+ (m/z
44) care genereaza un pic intens in spectru (Schema 3.21 calea a).
b). Transpozitia McLafferty
(Schema 3.21 calea b) are loc daca
exista un atom de hidrogen g in catena alchil, eliminandu-se o alchena si un cation radical de forma
RHC=C(OH)NH2![]() a
carui masa poate fi m/z=59, 73, 87 (pentru R=H, (CH2)nCH3
unde n=0, 1, 2).
a
carui masa poate fi m/z=59, 73, 87 (pentru R=H, (CH2)nCH3
unde n=0, 1, 2).
c). Scindarea legaturii s dintre atomii Cg-Cd cu eliminare de radical alchil si formarea unui cation a carui structura este probabil ciclica.
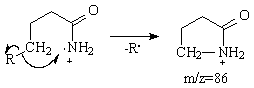
Principalele fragmentari in spectrul de masa al n-butiramidei sunt redate in Schema 3.21:
-ionul molecular al carui semnal este putin intens, sub 5%,
-picul de baza la m/z=59 generat printr-o transpozitie McLafferty (calea b):
-picul cu m/z=44, ( 68%) generat prin scindare a (calea a),
-picul cu m/z=72 generat prin eliminarea unui radical metil din ionul molecular (calea c).
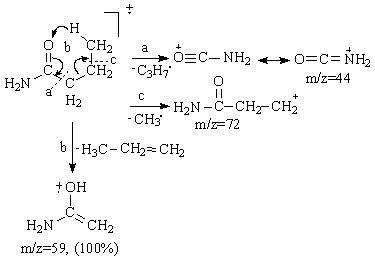
Schema 3.21
In cazul amidelor aromatice primare (ArCONH2) ionul molecular este intens si se poate fragmenta prin:
a). eliminarea unei o grupari NH2., conducand la ioni ArCO+ de intensitate mare, care se fragmenteaza ulterior cu eliminarea unei molecule neutre de monoxid de carbon si cation aril Ar+ (Schema 3.22 calea a).
b). scindare a cu eliminarea radicalului Ar. si aparitia picului cu m/z=44 corespunzand cationului CONH2+ (Schema 3.22 calea b).
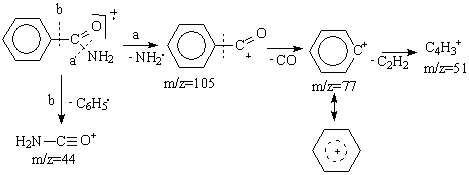
Schema 3.22
Principalele picuri in spectrul de masa al benzilamidei in ordinea scaderii intensitatii lor sunt: m/z=77 pentru cationul fenil, m/z=105 pentru cationul PhCO+, m/z=121 pentru ionul molecular, m/z=51 pentru cationul C4H3+ si m/z=44 pentru cationul CONH2+ (Schema 3.30). Picurile enumerate anterior au abundenta relativa mai mare de 50%, exceptie facand picul de la m/z=44 (sub 20%), deci scindarea a cu eliminarea radicalului Ar. este mai putin importanta.
In cazul amidelor alifatice secundare (RCONHR') si tertiare (RCONR'R") exista o serie de posibilitati de fragmentare, in functie de natura gruparilor R, R' si R".
a). Amidele cu un atom de hidrogen la carbonul g al gruparii acil si grupari metil la atomul de azot prezinta linii intense rezultate printr-o transpozitie McLafferty.
b). Amidele secundare se pot fragmenta prin scindarea legaturii amidice C-N, cu formarea unui cation acil.
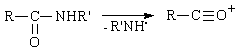
c). Amidele secundare si tertiare in care gruparile N-alchil sunt C2 sau mai lungi si gruparea acil este mai scurta decat C3, prezinta urmatorul mod de scindare: scindarea legaturii b C-C din radicalul N-alchil, urmata de scindarea legaturii C-N concomitent cu transpozitia unui hidrogen a (de la atomul de carbon atasat de gruparea acil) la atomul de azot (Schema 3.23).
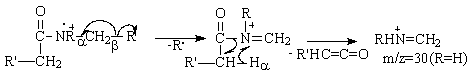
Schema 3.23
3.6.6.4 Anhidride
Principalele tipuri de fragmentare in cazul anhidridelor alifatice sunt prezentate in Schema 3.24:
a). scindarea legaturii C-O cu formarea cationului acil RC O+; acest cation are intensitate redusa, sau chiar lipseste din spectrul anhidridelor cu catena ramificata datorita posibilitatilor de scindare preferentiala a lantului alchilic, (calea a).
b). scindarea a oniu cu formarea cationului alchil R+, (calea b).
c). transpozitia McLafferty, (calea c).
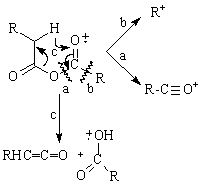
Schema 3.24
Anhidridele alifatice ciclice si cele aromatice prezinta in spectrul de masa picuri de tipul M-(CO2+CO). In cazul anhidridelor aromatice apar si picuri generate de ionii ArCO+, ArCO2H+ si M CO.
3.6.6.5 Cloruri acide
In spectrele de masa ale clorurilor si bromurilor acide, picul ionului molecular si picurile fragmentelor in care este prezent halogenul sunt insotite de picuri izotopice. Clorurile acide prezinta in spectrul de masa urmatoarele tipuri de fragmente: HCl+, COCl+ (generat prin scindarea a cu eliminarea radicalului alchil), RCO+sau ArCO+ (generate prin eliminarea unui atom de clor din ionul molecular).
3.6.7. NITRO DERIVATI
In cazul mono-nitro derivatilor alifatici picul ionului molecular este putin intens sau lipseste din spectru. Identificarea acestor derivati se poate face pe baza picurilor M-46, M-30 si m/z=30.
O cale importanta de fragmentare a nitroderivatilor alifatici este scindarea legaturii C-N cu formarea unui cation alchil -aparitia unui pic caracteristic M-NO2 (M-46) - care prin fragmentari ulterioare genereaza picuri caracteristice hidrocarburilor. In spectru apar si picuri pentru ionii NO+ (m/z= 30), NO2+ (m/z =46), M-OH si M-(OH+H2O).
In cazul nitro derivatilor aromatici picul ionului molecular este intens. Fragmentarea acestuia se realizeaza in principal prin:
a). eliminarea unui radical NO2, cu generarea unui pic la M 46, corespunzator radicalului aril, care se fragmenteaza cu eliminarea unei molecule de acetilena generand un pic intens la M-72 (Schema 3.25 calea a).
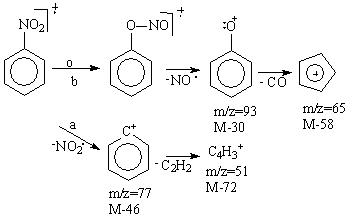
Schema 3.25
b). eliminarea unui radical NO. insotita de transpozitia oxigenului cu formarea forma cationului fenoxi la m/z=93, care se fragmenteaza cu eliminarea unei molecule de CO generand cationul ciclopentadienil la m/z=65, (Schema 3.25 calea b).
3.6.8. AMINE
Intensitatea ionului molecular si tipurile de fragmentari pe care aminele le prezinta in spectrele de masa sunt functie de natura aminei:
- amine alifatice cu lant ramificat sau linear,
- amine alifatice, aromatice sau mixte primare, secundare, tertiare.
In cazul aminelor alifatice liniare, ionul molecular este in general de intensitate slaba sau chiar este absent din spectru daca lantul alchil este lung sau puternic ramificat. Principalele cai de fragmentare sunt:
a). Scindarea legaturii C-C dispusa in pozitia b fata de azot cu eliminarea unui radical alchil, (in cazul aminelor secundare si tertiare se elimina preferential radicalul cu catena cea mai mare), si a unui cation de tipul R2C=NR2 . In cazul in care aminele nu sunt ramificate la atomul de carbon a, cationul R2C=NR2 este cel mai abundent din spectru (pic de baza), (Schema 3.26 pentru R = alchil).
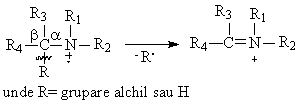
Schema 3.26
b). Daca in molecula aminei exista un atom de hidrogen a (hidrogen la atomul de carbon direct legat de azot) in spectrul de masa este vizibila de obicei o linie la M 1, generata prin eliminarea acestui atom, (Schema 3.26 pentru R = H).
c). In cazul aminelor primare cu catene alifatice liniare mai lungi de cinci atomi de carbon apar fragmentari cu eliminarea unor radicali alchil si formarea unor cationi ciclici a caror masa este m/z=72 pentru n=1, si 86 pentru n=2.

d) In spectru apar de asemenea si cationi CnH2n+1, CnH2n si CnH2n alaturi de cationi in care sarcina ramane la fragmentul ce contine atomul de azot, generate prin scindarea legaturilor C C b g d e, etc. din lantul alchilic.
In cazul aminelor ciclice, linia ionului molecular este de obicei intensa, cu exceptia cazului in care exista un substituent in pozitie a. Fragmentarile ce apar in acest caz sunt:
a). Dubla scindare a, care in acest caz se concretizeaza prin ruperea legaturilor b C-C de ambele parti ale azotului, (Schema 3.27).

Schema 3.27
b). Pierderea unui atom de hidrogen de tip a generand un pic M 1 intens.
In spectrul de masa al N-metil pirolidinei, (Schema 3.27 R=CH3), sunt prezente urmatoarele picuri m/z=85 pentru ionul molecular, m/z=84 generat de pierderea unui atom de hidrogen, m/z=57 generat printr-o dubla scindare a de ambele parti a azotului si m/z=42 care este si pic de baza. Cu exceptia ionului molecular picurile mentionate anterior au o abundenta relativa mai mare de 80%.
In cazul aminelor aromatice picul ionului molecular este intens. In spectrul de masa al anilinei cele mai intense picuri sunt: M, M-HCN, M-(HCN+H) si M-1, (Schema 3.28).

Schema 3.28
In cazul anilinelor substituite la nucleu cu grupe alchil, (Schema 3.29), principala fragmentare consta intr-o scindare a legaturii C-C, dispuse in b fata de nucleul aromatic, concomitent cu transpozitia gruparii metil cu formarea unui radical alchil si a unui cation amino-tropiliu.
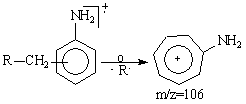
Schema 3.29
In cazul alchilarilaminelor, principala fragmentare consta in ruperea legaturii C C b fata de atomul de azot, (Schema 3.29).
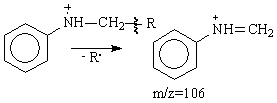
Schema 3.29
3.6.9. COMPUSI HETEROAROMATICI
Linia ionului molecular al compusilor heteroaromatici si al compusilor heteroaromatici alchilati este intensa. Principala cale de fragmentare este scindarea legaturii b fata de ciclul aromatic, ca in alchilbenzeni, cu localizarea sarcinii la heteroatom.
3.6.9.1 Furan, Tiofen, Pirol
Heterociclurile aromatice formate din cinci atomi (furan, tiofen, pirol) prezinta moduri similare de fragmentare ale ciclului. Primul pas, in fiecare caz, este scindarea legaturii carbon-heteroatom, (Schema 3.30).
Astfel, furanul prezinta doua linii principale: C3H3+ (m/z 39) si HCºO+ (m/z 29).
Pentru tiofen, exista trei linii principale: C3H3+ (m/z 39), HCºS+ (m/z 45) si C2H2S+. (m/z 58).
Pirolul prezinta trei linii: C3H3+ (m/z 39), HCºNH+ (m/z 28) si C2H2NH+. (m/z 41). Pirolul elimina de asemenea o molecula neutra de HCN pentru a da o linie intensa la m/z 40.

Schema 3.30
3.6.9.2 Piridine
In cazul heterociclurilor hexa-atomice cu azot, ca de exemplu piridina, principala cale de fragmentare este eliminarea unei molecule de acid cianhidric. In cazul piridinelor substituite la nucleu cu grupe alchil apar fragmentari b g d ale catenei alchil, transpozitii Mc. Lafferty, iar pentru piridinele substituite in pozitia 2 apare o scindare a insotita de o transpozitie nespecifica a unui atom de hidrogen, din catena alchil, la pozitia 2 a ciclului aromatic. Preferinta pentru fragmentari b g d ale catenei alchil si transpozitii Mc. Lafferty este functie de pozitia gruparii alchil pe ciclu.
3.6.9.3 Fenotiazine
Alcoxi fenotiazine
Studiile spectroscopice de masa in clasa hidroxifenotizinelor, respectiv metoxifenotiazinelor au permis identificarea regioizomerilor, in functie de abundenta relativa a ionilor si a diferentelor ce pot aparea in procesul de fragmentare a acestora.
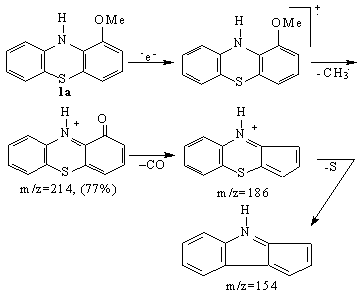
J.C. Craig (J.C. Craig, L.R. Krai, Tetrahedron, 1968, 24, 4267-4276) a studiat comportarea sub impactul electronic a unor metaboliti fenotiazinici izolati din organismul pacientilor tratati cu promazina sau clorpromazina, cat si metoxi-, respectiv hidroxifenotiazine nealchilate la atomul de azot. Spectrele de masa ale 1-metoxi-, respectiv 3-metoxifenotiazina sunt similare dar s-au constatat diferente cantitative, acestea permitand diferentierea celor doi regioizomeri. Astfel, ionul asociat cu pierderea radicalului metil din ionul molecular este dublu in intensitate in 1-metoxifenotiazina 1a fata de 3-metoxifenotiazina 1b.
Ambele substante elimina succesiv in procesul de fragmentare: un radical metil, monoxid de carbon si un atom de sulf (Schema 3.31).
Ambele spectre au un pic cu abundenta relativa de 100% corespunzator ionului molecular (pic de baza), ceea ce dovedeste stabilitatea ridicata a inelului fenotiazinic. Semnalul urmator, cu o abundenta relativa de 77% pentru 1-metoxifenotiazina, respectiv 50% pentru 3-metoxifenotiazina, apare la m/z 214 si se datoreaza pierderii radicalului metil.
Studiul spectrelor de masa pentru 3-metoxi, 7-metoxi, respectiv 8-metoxi-2-clorofenotiazine 2a,b,c, a aratat diferente in ceea ce priveste abundenta relativa a picurilor cu aceeasi masa cat si absenta unor semnale la unii dintre izomeri. Aceste diferente au permis diferentierea regioizomerilor, cat si studiul influentei pozitiei grupelor metoxi- asupra tipului de fragmentare.

Schema 3.3
Tinand cont de pozitia semnalelor si abundenta lor relativa, se poate prezenta o schema de fragmentare comuna a acestor regioizomeri 2a,b conform schemelor 3.32 a. si 3.32 b.
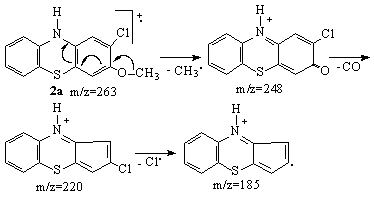
Schema 3.32 a.
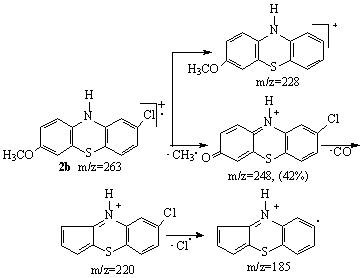
Schema 3.32 b.
Analiza spectrelor de masa a permis formularea urmatoarelor concluzii:
Pierderea radicalului metil din ionul molecular este o caracteristica comuna celor trei regioizomeri, formandu-se un pic la m/z 248, a carui abundenta relativa este 74% pentru 3-metoxi-2-clorofenotiazina 2a, 42% pentru 7-metoxi-2-clorofenotiazina 2b, respectiv 21% pentru 8-metoxi-2-clorofenotiazina 2c. Din ionul rezultat, procesul de fragmentare continua cu eliminarea succesiva a unei molecule de monoxid de carbon, urmata de pierderea unui atom de clor.
Din spectrul 3-metoxi-2-clorofenotiazinei 2a, lipseste picul de la m/z 228 M-Cl, semnal ce are abundenta relativa de 1% pentru 2b, respectiv 10% pentru 2c.
Hidroxifenotiazine
In acelasi context au fost studiate si hidroxi-2-clorofenotiazinele 3a-d, cu grupare hidroxil in pozitia: 3, 6, 7 si 8. S-au constatat diferente semnificative intre spectrul de masa al 3-hidroxi-2-clorofenotiazinei 3a si spectrele celorlalte trei hidroxifenotiazine 3b-d, dar numai diferente minore intre spectrele izomerilor 3b-d.
De exemplu, in spectrul 3-hidroxi-2-clorofenotiazinei 3a picurile de la m/z 220 si m/z 188 au o abundenta relativa mica, in comparatie cu cele ale celorlalti izomeri. Pentru a diferentia intre ele hidroxifenotiazinele 3b-d, s-a impus examinarea atenta a spectrelor de masa. Pe baza abundentei relative a picului de la m/z 180 s-a putut diferentia 7-hidroxi-2-clorofenotiazina 3c de izomerii de pozitie 3b, d.
Schema de fragmentare a hidroxifenotiazinelor 3a-d, este general valabila acestei clase si poate fi exemplificata pentru oricare dintre izomeri (Schema 3.33).
Din spectrele de masa se constata ca fragmentarea ionului molecular pentru 8-hidroxi-2-clorofenotiazina 3d decurge pe trei cai.
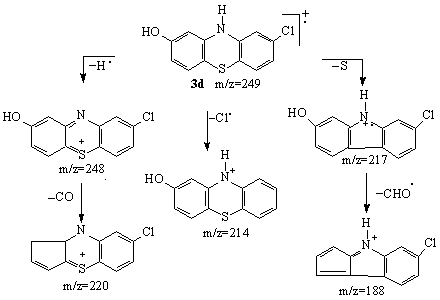
Schema 3.33
Prima fragmentare consta in pierderea unui atom de hidrogen din ionul molecular, rezultand un pic cu m/z 248. Eliminarea atomului de hidrogen se face de la azotul din ciclu si nu de la gruparea hidroxil. Confirmarea acestei afirmatii este data de prezenta in spectrele metoxiderivatilor 1a,b si 2a-c, a unui ion de masa M-1, cat si de absenta ionului de tip M-1 din spectrele hidroxi-2-cloropromazinelor 4a,b (vezi Schema 3.33).
Expulzarea unei molecule de monoxid de carbon din ionul de masa m/z 248 explica prezenta picului de la m/z 220.
Urmatoarele doua variante de fragmentare a ionului molecular constau in:
- eliminarea unui atom de clor, ducand la aparitia ionului de masa m/z 214
- eliminarea unui atom de sulf, ducand la aparitia ionului de masa m/z 217. In continuare, fragmentarea acestuia se face cu eliminarea unui radical de tip CHO. , rezultand un ion inregistrat la valoarea m/z 188.
In cazul hidroxi-2-cloropromazinelor 4a-d, ale caror grupari hidroxil se afla in una dintre pozitiile 3,6,7, sau 8, picurile cu abundenta relativa maxima se obtin la valori m/e 58, fiind urmate de cele de la valori m/e 85 si pot fi atribuite ionilor 4a',a'' indiferent de pozitia gruparii hidroxil (Schema 3.34).
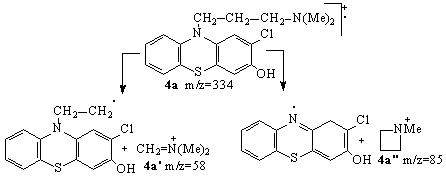
Schema 3.34
Celelalte picuri din spectrul de masa pot fi atribuite fragmentarii ionului molecular cu eliminarea catenei dimetilaminopropil din pozitia 10, rezultand un ion cu masa m/z 248, procesul de fragmentare continuand cu eliminarea de monoxid de carbon m/z 220 si a atomului de clor.
O diferenta semnificativa intre spectrele de masa ale 3-hidroxi derivatului 4a si 6-hidroxi-, 7-hidroxi-, respectiv 8-hidroxi-2-cloropromazinelor 4b-d, este absenta ionilor de masa m/z 289 si 288 din spectrul 3-hidroxiderivatului 4a. Acestor ioni le pot fi atribuite structuri ciclice sau lineare ale catenei alchil (Schema 3.35).
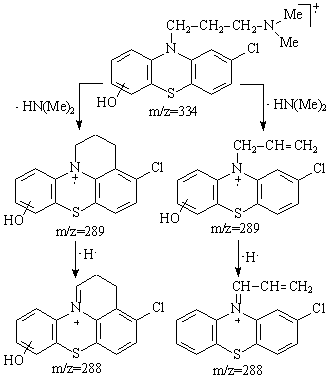
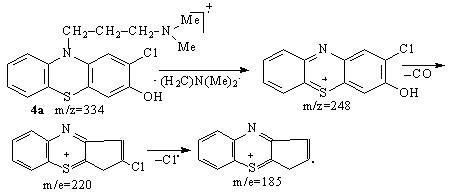
Schema 3.35
Studiind comportarea la impactul cu fluxul electronic a hidroxifenotiazinelor respectiv metoxifenotiazinelor (Schemele 3.31-3.35), se constata stabilitatea nucleului fenotiazinic la fragmentare, cat si preferinta, de fragmentare diferentiata sau doar abundente relative diferite a unor ioni, in functie de pozitia pe nucleu a gruparilor hidroxi, respectiv metoxi.
Mital (M.D. Sadhnani, N.L. Agarval, R.L. Mital, Bull. L'Acad. Polon. Scienc. 1973, XXI (12), 878-873) a studiat pe o serie de hidroxi-polihalofenotiazine comportarea la impactul cu fluxul electronic si influenta substituentilor asupra cailor de fragmentare. In majoritatea cazurilor ionul molecular este pic de baza, confirmand stabilitatea ridicata a nucleului fenotiazinic, la impactul cu fluxul electronic.
Picurile din spectru, a carora le corespund ionii cu masa M-32 sunt rezultate prin expulzarea unui atom de sulf din ionul molecular, iar abundenta lor relativa este mai mare la hidroxi-clorofenotiazine decat la derivati fluorurati sau bromurati.
Picul de masa M-1 a fost atribuit ionului generat prin expulzarea hidrogenului direct legat de azot. Ionul astfel generat se scindeaza prin eliminare de monoxid de carbon, urmata de eliminare de halogen. Aceasta cale de fragmentare este comuna pentru derivatii hidroxi-polihalo-fenotiazinici, deci poate fi exemplificata in cazul particular al 1,2,4,7-tetracloro-3-hidroxifenotiazinei (Schema 3.36).
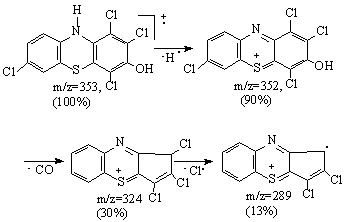
Schema 3.36
a. scindarea din ionul molecular a legaturii CAlif-O, cu eliminarea unui radical alchil si formarea ionilor de masa m/z 184.
b. scindarea din ionul molecular a legaturii CAlif-O, insotita de transpozitia unui proton la oxigen si formarea radical cationului m/z 185 corespunzator 3-hidroxidifenilaminei, (transpozitie Mc. Lafferty).
c. eliminarea din 3-hidroxidifenilamina a unui radical HO. si formarea unui pic la m/z=168.
d. fragmentarea cu eliminarea unui radical formil din ionul de masa m/z 185 sau a unei molecule de monoxid de carbon din ionul de masa m/z 184, duce la ionul de fragmentare m/z 156, in acest caz de intensitate scazuta.

Schema 3.37

Fig.3. 4. Spectrul de masa al 3-dodeciloxidifenilaminei
2. In spectrele de masa ale bazelor Schiff (de exemplu in spectrul de masa al N-(10-etilfenotiazin-3-metiliden)-m-toluidinei reprezentat in figura 3.5), pe langa picul molecular apare si un pic izotopic de masa M+1. Intensitatea mare a acestuia din urma este datorata izotopilor: 13C, 2H, 15N, 17O prezenti in molecula.
Analiza spectrelor de masa ale Bazelor Schiff derivate de la 10-etil-3-formilfenotiazina sugereaza urmatoarele cai de fragmentare:
- eliminarea radicalul etil substituent al atomului de azot din structura heterociclului fenotiazina (schema 3.38 calea c), cu formarea unui pic la m/z=315.
- ionul de fragmentare de masa m/z 226, este generat de scindarea legaturii dintre inelul fenotiazinic si substituentul din pozitia 3 (Schema 3.38 calea b)
- picul de masa m/e 91 apartine ionului tropiliu C7H7+, si este caracteristic fragmentarii compusilor aromatici alchilati conform schemei 3.38, calea a.
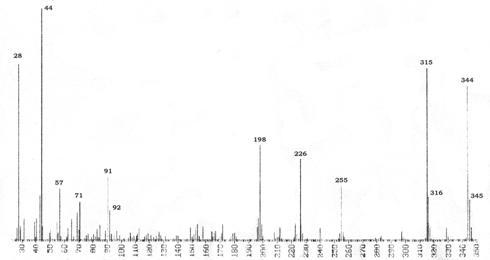
Fig. 3.5. Spectrul de masa al N-(10-etilfenotiazin-3-metiliden)-m-toluidinei
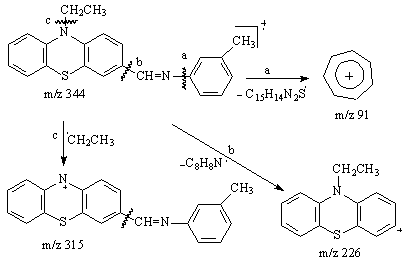
Schema 3.38
In spectrul N-(10-metilfenotiazin-3-metiliden)-m-nitroanilinei apare fragmentul de masa m/z 213, ca rezultat al formarii unui radical cation de tip 10-metilfenotiazinil, prin procesul de fragmentare a ionului molecular (Schema 3.39, calea b).
In spectrele compusilor ce contin gruparea nitro, apare picul de masa M-30 (M-NO), caracteristic nitroderivatilor aromatici. Gruparea nitro sufera un proces de transpozitie la grupare nitrit din care se scindeaza apoi radicalul nitrozil. De asemenea in spectru apare si picul de masa M-46 datorat eliminarii unui radical nitro (NO2), dar intensitatea lui este redusa.
Formarea unui pic la m/z=315 se datoreaza eliminarii radicalului etil de la azotul fenotiazinic (Schema 3.39, calea c).
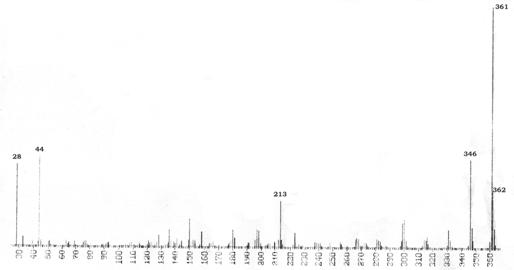
Fig. 3.6. Spectrul de masa al N-(10-metilfenotiazin-3-metiliden)-m-nitroanilinei

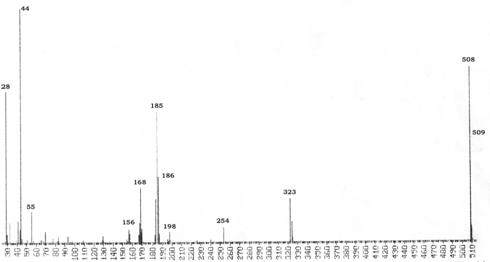
Fig. 3.7 Spectrul de masa al 3-dodeciloxidifenilaminei

Schema 3.40
Din ionul molecular si din ionii de fragmentare au loc mai multe tipuri de scindari:
a. Scindare a, ce presupune ruperea legaturii C-C dispusa in b fata de oxigen, si conduce la picul m/z 198, (Schema 3.40, calea a).
b. Scindarea legaturii C-O, insotita de transpozitia unui atom de hidrogen, din catena alchil, la oxigen conduce la formarea ionului de masa m/z 185. Procesul este urmat fie de eliminarea unui radical CHO. si formarea ionului cu masa m/z 156, fie de eliminare unui radical HO. cand se formeaza un cation de masa m/z 168, (Schema 3.40, calea b).
c. In cazul in care din ionul molecular se elimina 3-hidroxidifenilamina sub forma de molecula neutra, se formeaza radical cationi de masa m/z 323, iar acestia prin scindarea catenei alchil genereaza cationul cu m/z=254 (Schema 3.40, calea c).
3.8. PROBLEME
Spectrul de masa al 3-octiloxidifenilaminei redat in figura 3.8, prezinta picuri la valorile m/z= 298, 297, 185, 184, 168, 156. Atribuiti acestor picuri structura ionilor care le-au generat.
Rezolvare:
Spectrul de masa prezinta picul molecular la m/z= 298, alaturi de picul izotopic de m/z= 297. Picurile de la m/z= 185, 184, 168,si 156 au fost generate prin urmatoarele tipuri de fragmentari, schema 3.41:
a. scindarea din ionul molecular a legaturii CAlif-O, cu eliminarea unui radical alchil si formarea ionilor de masa m/z 184.
b. scindarea din ionul molecular a legaturii CAlif-O, insotita de transpozitia unui proton la oxigen si formarea radical cationului m/z 185 corespunzator 3-hidroxidifenilaminei, (transpozitie Mc. Lafferty).

Schema 3.41
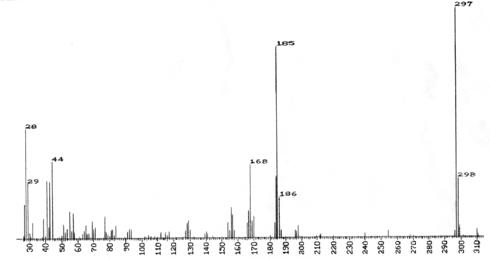
Fig. 3.8 Spectrul de masa al 3-octiloxidifenilaminei
c. eliminarea din 3-hidroxidifenilamina a unui radical HO. si formarea unui pic la m/z=168.
d. fragmentarea cu eliminarea unui radical formil din ionul de masa m/z 185 sau a unei molecule de monoxid de carbon din ionul de masa m/z 184, duce la ionul de fragmentare m/z 156, in acest caz de intensitate scazuta.
In figurile 3.9 3.10si 3.11sunt prezentate spectrele de masa a trei derivati substituiti ai fenotiazinei, care au in comun acelasi substituent in pozitia 3 a nucleului aromatic. Se mai stie ca:
- Derivatul fenotiazinic a nu mai are nici un alt substituent in afara celui din pozitia 3 si prezinta urmatoarele picuri caracteristice: 227, 226, 198, 166.
- Derivatul fenotiazinic b prezinta pe langa substituentul din pozitia 3 un substituent la atomul de azot si in spectru apar urmatoarele picuri: 241, 226, 197, 212, 180.
- Derivatul fenotiazinic c este disubstituit si prezinta urmatoarele picuri caracteristice: 251, 260, 232, 200 si 197.
Care sunt formulele structurale ale celor trei derivati substituiti ai fenotiazinei si explicati care este modul de fragmentare al fiecaruia ?
Numerotarea pozitiilor atomilor din heterociclul fenotiazina este:
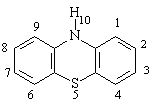
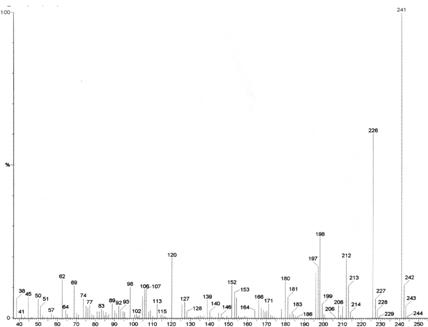 m/z
m/z
Fig. 3.9 Spectrul de masa al derivatului fenotiazinic a din problema 3
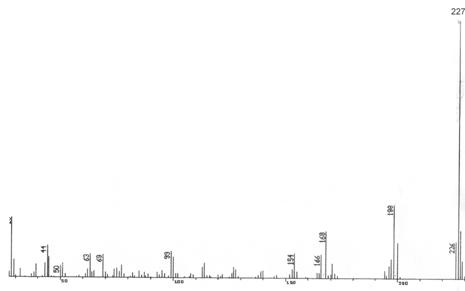 m/z
m/z
Fig. 3.10 Spectrul de masa al derivatului fenotiazinic b din problema 3
 m/z
m/z
Fig. 3.11 Spectrul de masa al derivatului fenotiazinic c din problema 3
Rezolvare:
Pentru identificarea gruparilor functionale prezente pe nucleul fenotiazinic se face diferenta dintre valoarea m/z corespunzatoare picului molecular corespunzatoare compusilor a b c respectiv masa moleculara a fenotiazinei monosubstituita (pentru compusul a) si disubstituita (pentru compusul b si c).
In cazul compusului a, se gaseste masa moleculara a gruparii grefate pe nucleul fenotiazinic ca fiind de 29, aceasta corespunde gruparii formil CH=O. Conform datelor problemei aceasta grupare este comuna derivatilor b si c. Stiind masa moleculara a compusului a prin diferenta intre aceasta si valorile m/z pentru picurile moleculare a compusilor b, c se gasesc valorile maselor moleculare a fragmentelor grefate suplimentar pe nucleul fenotiazinic. Astfel in structura compusului b se gaseste un radical cu masa moleculara de 15 ce corespunde gruparii CH3, iar in compusul c un radical cu masa de 35 ce corespunde unui atom de clor.
Cele trei fenotiazine sunt: a 10-H-3-formilfenotiazina (Schema 3.42), b 10-metil-3-formilfenotiazina (Schema 3.42), c 10-H-3-formil-2-clorofenotiazina (Schema 3.42).
In spectrul de masa din figura 3.9 ionul molecular al compusului a (10-H-3-formilfenotiazina) se fragmenteaza in principal prin:
- eliminarea unui radical formil, cu formarea picului m/z=198 care prin eliminare de sulf conduce la picul cu m/z=166.
- eliminarea unui atom de hidrogen cu formarea picului cu m/z=226.
In spectrul de masa din figura 3.10 ionul molecular al compusului b (10-metil-3-formilfenotiazina) se fragmenteaza in principal prin:
- eliminarea unui radical formil, cu formarea picului m/z=212 din care prin eliminare de sulf rezulta picul cu m/z=180, iar prin eliminarea gruparii metil picul m/z= 197.
- eliminarea unui radical metil cu formarea picului cu m/z=226, care poate pierde un radical formil, cu formarea picului m/z=197.
In spectrul de masa din figura 3.11 ionul molecular al compusului c (10-H-3-formil-2-clorofenotiazina) se fragmenteaza in principal prin:
- eliminarea unui radical formil, cu formarea picului m/z=232 din care prin eliminare de sulf rezulta picul cu m/z=200, iar prin eliminarea unui atom de clor picul m/z= 197.
- eliminarea unui atom de hidrogen cu formarea picului cu m/z=260.

Schema 3.42
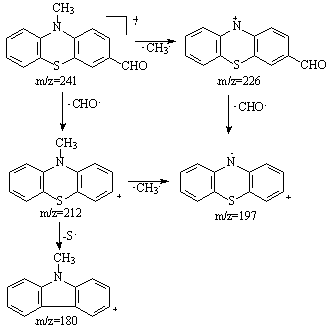
Schema 3.42

Schema 3.42
. Propuneti o formula structurala pentru compusul cu formula moleculara C6H6O, care in spectrul de masa prezinta linii la valorile m/z=66 si m/z=65. Descrieti structura cea mai probabila a fiecaruia dintre aceste fragmente.
Rezolvare:
Compusul este fenolul si de fragmenteaza prin eliminarea succesiva a unei molecule de CO (m/z=66) si a unui atom de hidrogen (m/z=65). Schema de fragmentare este:
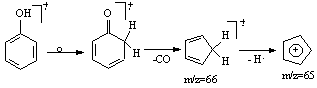
. Care este formula structurala a compusului cu formula moleculara C7H8, care in spectrul de masa prezinta fragmente cu masa m/z= 91 si 65. Descrieti structura cea mai probabila a fiecaruia dintre aceste fragmente.
Rezolvare:
Compusul este toluenul si se fragmenteaza cu eliminarea unui atom de hidrogen generand ionul tropiliu m/z=91, pic caracteristic alchil benzenilor.
Schema de fragmentare este:

. Care este formula structurala a compusului cu formula moleculara C7H7NO care prezinta in spectrul de masa linii caracteristice situate la valori m/z=105, 77, 51, 44. Descrieti structura cea mai probabila a fiecaruia dintre aceste fragmente.
Rezolvare:
- ansamblul de picuri cu m/z 71 - 51 este caracteristic derivatilor monosubstituiti ai benzenului.
- picul de la m/z=105 se obtine prin eliminarea unui radical cu masa 16 corespunzator unei grupari -NH2 iar picul de la m/z= 77 este generat prin eliminarea unui fragment cu masa 28 (corespunzator unei molecule neutre de CO) din picul cu m/z=105.
- cunoscand formula moleculara putem calcula masa moleculara si implicit valoarea m/z pentru ionul molecular. Din aceasta se scade masa gruparii fenil si se determina masa radicalului grefat pe nucleul benzenic, aceasta are valoarea de 44, valoare care se obtine si prin insumarea maselor moleculare ale gruparilor -NH2 si CO. In concluzie compusul este benzamida iar schema de fragmentare este:
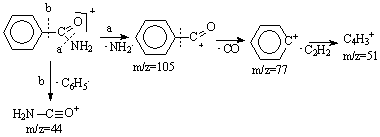
|