Acoperiri cu straturi organice. Polimeri conductori si neconductori utilizati in protectia anticoroziva
Scopul lucrarii
Depunerea unor straturi compacte polimerice (polifenol si polipirol) pe suport de otel in scopul protectiei anticorozive.
Verificarea proprietatilor protectoare ale straturilor obtinute.
Introducere
Protectia suprafetelor metalice cu pelicule organice
Unul dintre cele mai intens studiate domenii din electrochimie in ultimii zece ani il constituie electrozii cu suprafata modificata cu polimeri conductori sau neconductori. Utilizarea acestora in diverse domenii a deschis noi perspective si noi abordari in domeniul electrochimiei.
Proprietatile protectoare ale straturilor organice, impotriva coroziunii sunt cunoscute in literatura stiintifica de specialitate. Permanent au existat preocupari pentru marirea capacitatii protectoare a peliculelor prin intrebuintarea de materiale peliculogene cu capacitate de imbibare redusa, cu permeabilitate mica la apa si gaze si care sa prezinte un proces de imbatranire incetinit, cat si pentru gasirea celor mai optime tratamente ale suportului metalic care sa asigure maximum de aderenta intre pelicula si metal.
Rezistenta anticoroziva a protectiilor cu pelicule organice este dependenta de natura, calitatea, compactitatea peliculei, de prelucrarea suportului metalic, de aderenta peliculei la suport, precum si de modul de intretinere a peliculei.
Polimerii pot fi obtinuti in doua moduri:
- polimerizare chimica;
- polimerizare electrochimica;
In cele ce urmeaza se va prezenta doar obtinerea polimerilor prin polimerizare electrochimica.
Acoperiri cu polimeri necoductori polifenol
Schematic, oxidarea electrochimica a fenolului, decurge cu formarea radical cationilor fenoxid in prima etapa. Acestia sunt specii puternic acide, instabile care sufera o deprotonare rapida si apoi cuplarea cu formarea unor dimeri, trimeri si chiar structuri polimerice care raman adsorbite pe suprafata electrodului, blocandu-l total (reactiile din figura 4.3.1.)
![]() (1)
(1) ![]() (2)
(2)
![]() (3)
(3)
Fig. 4.3.1 Prezentarea schematica a mecanismului de oxidare a fenolului
Pentru procesul de oxidare a compusilor fenolici pe electrozii metalici este propus urmatorul mecanism de reactie, prezentat in Fig. 4.3.2.

Fig. 4.3.2 Mecanismul propus pentru oxidarea electrochimica a fenolului
In prima etapa a mecanismului are loc oxidarea fenolului cu obtinerea radical cationilor fenoxid, care sunt acizi foarte puternici si care se deprotoneaza rapid cu formarea radicalului neutru. Din aceasta faza reactia poate urma doua cai:
radicalii fenoxid adiacenti adsorbiti pe suprafata electrodului se pot cupla prin formare de dimeri, trimeri sau chiar structuri polimerice care raman adsorbiti pe electrod blocandu-i astfel suprafata (figura 4.3.2 varianta A);
radicalii obtinuti pot suferi o noua oxidare cu formare de hidrochinona si apoi benzochinona (figura 4.3.2 varianta B).
Polimerizarea fenolului pe suprafata electrozilor metalici determina formarea unui strat protector impotriva coroziunii.
Acoperiri cu polimeri conductori - polipirol
Polimerizarea electrochimica a pirolului decurge dupa schema prezentata in figura 4.3.3. Polimerizarea pirolului duce la obtinerea unui sistem conjugat de electroni ce permite deplasarea libera a acestora determinand caracterul de polimer conductor al acestuia.
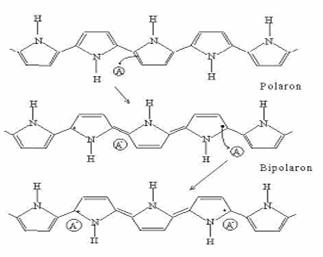
Fig. 4.3.3 Schema de polimerizarea electrochimica a pirolului
Metode de lucru utilizate pentru polimerizarea electrochimica:
Metoda polarizarii potentiostatice pentru trasarea curbelor de polarizare i = f(timp) (i = densitate de curent).
Metoda galvanostatica pentru trasarea curbelor de polarizare E=f(timp) (E = potential).
Metoda polarizarii potentiodinamice utilizata la trasarea voltamogramelor ciclice (presupune variatia ciclica a potentialului si inregistratrarea curentului corespunzator).
Atat curbele potentiostatice cat si voltamogramele permit determinarea principalilor parametri electrochimici ce caracterizeaza procesul de coroziune si anume: Ecor - potential de coroziune; icr - curent critic (maxim) de coroziune; Ep - potential (primar) de pasivare; Epc - potential de pasivare completa; Epitt - potential de pitting; Er,pitt - potential de repasivare a pittingului; ET - potential de transpasivitate; ip - curent de pasivitate.
Metoda polarizarii liniare consta in determinarea dependentelor E-i pentru un domeniu de polarizare de maximum 10[mV] in jurul potentialului de coroziune, in scopul determinarii rezistentei de polarizare.
Polimerizarea fenolului
Mod de lucru
Se curata suprafata piesei de otel cu hartie abraziva, se spala in jet de apa;
Se imerseaza cate 5 minute in solutia de degresare, se spala in jet de apa;
Se imerseaza 5 minute in solutia de decapare, se spala cu apa distilata si se usuca cu hartie de filtru;
Se cantareste placuta de otel la balanta analitica cu precizie de 0.0001 g si se noteaza masa initiala, mi;
Se monteaza electrozii in suport, se conecteaza la bornele electrolizorului respectand polaritatile si se introduc in baia de electroliza;
Se conecteaza instalatia de electroliza la retea si se pune in functiune;
Se realizeaza o curba de polarizare la ±150 [mV] fata de potentialul OCP, la o viteza de 2[mV/s] in clorura de sodiu 3%;
Se determina potentialul de coroziune si curentul de coroziune prin metoda Tafel;
Se scot electrozii si se spala cu apa distilata;
Se curata suprafata piesei de otel cu hartie abraziva, se spala in jet de apa;
Se imerseaza cate 5 minute in solutia de degresare, se spala in jet de apa;
Se imerseaza 5 minute in solutia de decapare, se spala cu apa distilata si se usuca apoi cu hartie de filtru;
Se cantareste placuta de otel la balanta analitica cu precizie de 0.0001 g si se noteaza masa initiala, mi;
Se polimerizeaza galvanostatic la 0.1 [mA/cm2] timp de 30 minute in solutia de fenol 0.1M in 1mM sulfat de sodiu;
Se scot electrozii, se spala cu apa distilata, apoi se usuca prin tamponare cu hartie de filtru;
Se cantareste placuta de otel la balanta analitica cu precizie de 0.0001 g si se noteaza masa finala, mf.
Se calculeaza masa de fenol depusa electrochimic;
Se realizeaza o curba de polarizare la ±150 [mV] fata de potentialul de echilibru in clorura de sodiu 3%;
Se determina potentialul de coroziune si curentul de coroziune prin metoda Tafel.
Interpretare rezultate Se compara valorile cu cele obtinute pe electrodul netratat.
|