Forta electromotoare a pilei Daniell-Jacobi
Se determina dependenta fortei electromotoare a pilei Daniell-Jacobi în functie de concentratia solutiei de electrolit si se calculeaza constanta de echilibru pentru procesul electrochimic din pila.
Pilele electrochimice (sau elemente galvanice) sunt dispozitive în care, în procesele electrochimice, energia chimica se transforma în energie electrica.
Pilele electrochimice sunt alcatuite din doua semielemente unite printr-o punte de sare sa 12512b120m u diafragma care împiedica amestecarea electrolitilor dar permite trecerea ionilor între cele doua semielemente.
Fiecare semielement este format dintr-un electrod:
anodul (-) este electrodul cu potentialul de electrod de reducere mai negativ unde are loc reactia de oxidare;
catodul (+) este electrodul cu potentialul de reducere mai pozitiv unde are loc reactia de reducere.
Pila Daniell-Jacobi este o pila electrochimica reversibila, reprezentata prin urmatorul lant electrochimic:
(-) Zn / ZnSO4 (a1) // CuSO4 (a2) / Cu (+) (4.16)
Când circuitul electric este închis la electrozi au loc simultan urmatoarele reactii electrochimice care genereaza curentul electric:
Anod (-): ![]() (4.17)
(4.17)
Catod (+):![]() (4.18)
(4.18)
Reactia globala: ![]() (4.19)
(4.19)
Tensiunea electromotoare E a unei pile electrochimice este diferenta dintre potentialele de electrod ale catodului, ec si anodului, ea
E = e e ec ea (4.20)
Valorile numerice ale potentialului de electrod sunt date de relatia lui Nernst:
![]() (4.21)
(4.21)
![]() (4.22)
(4.22)
în care: e este
potentialul de electrod standard; R,
constanta universala a gazelor ideale, F,
constanta lui Faraday (F = 96487,3
C/Eg = 23062,9 cal/V.Eg); n,
numarul de electroni transferati în reactia redox; T,
temperatura absoluta (K); a, activitatea termodinamica (a = f∙c; unde c este concentratia solutiei de electrolit iar f, coeficientul de activitate). Pentru
solutii foarte diluate ![]() deci
deci ![]() Pentru metale pure a =
1.
Pentru metale pure a =
1.
Tensiunea electromotoare a pilei respecta relatia lui Nernst:
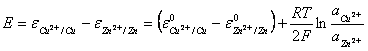 (4.23)
(4.23)
Forta electromotoare standard a pilei este:
![]() (4.24)
(4.24)
La temperatura de 298 K relatia (4.23) devine:
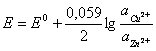 (4.25)
(4.25)
Din relatia (8) rezulta ca tensiunea electromotoare a unei pile depinde de concentratiile electrolitilor de la cei doi electrozi, de temperatura si de numarul de electroni implicati în procesul redox.
Lucrul electric produs de un element galvanic la presiune si la temperatura constanta este:
![]() (4.26)
(4.26)
si ![]() (4.27)
(4.27)
Pentru DG < 0 sau ( E > 0) reactia electrochimica din pila are loc spontan, deci elementul galvanic debiteaza curent electric.
Constanta de echilibru pentru procesul electrochimic din pila reversibila se poate determina pe baza entalpiei libere de reactie:
![]() (4.28)
(4.28)
Combinând
relatiile (4.26) si (4.27) rezulta: ![]() (4.29)
(4.29)
Electrod de zinc, electrod de cupru, punte de sare sau banda de hârtie de filtru umezita în electrolit, milivoltmetru electronic.
Modul de lucru
Electrolit
Coeficient de activitate
0,001M
0,01M
0,05M
0,1M
0,5M
1M
CuSO4
ZnSO4
Pila electrochimica
Eexp,
V
Ecalc,
V
DE,
V
I
II
III
IV
V
Se reprezinta grafic
dependenta E = f (cZn2+) pentru ![]() si se
discuta.
si se
discuta.
|